
QUIMICA Y DROGAS

SUSTANCIAS QUIMICAS UTILIZADAS EN LA PRODUCCION
ILICITA DE DROGAS
ACIDO BUTIRICO
Usos lícitos: disolvente de diversas sustancias
(nitrocelulosa, barnices, lacas); en la preparación de aromas artificiales de
frutas; en la fabricación de pólvora sin humo, de cuero y seda artificiales, y
de perfumes.
ACETATO
ISOPROPILICO
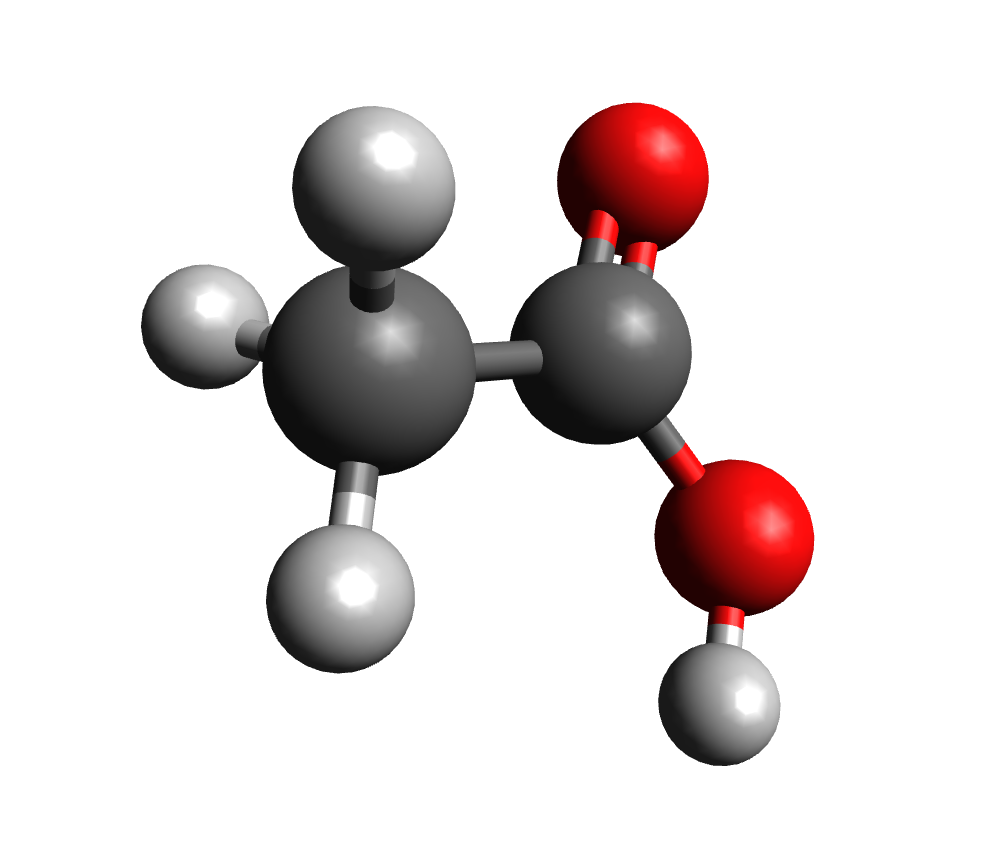
Otros nombres: Acido etanoico, ácido metanocarboxílico; ácido del vinagre.
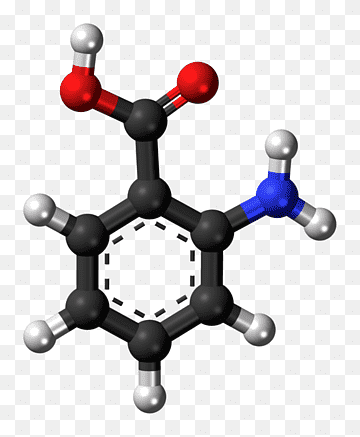
Observaciones: El ácido N-acetilantranílico es el procursor
inmediato que se emplea en la síntesis de la metacualona y meclocualona. A su vez, se prepara a menudo a partir del
ácido antranílico. Ciertos ésteres del
ácido N-acetilantranílico, por ejemplo, la ajacina, están ahora fiscalizados
conforme a la CSA.
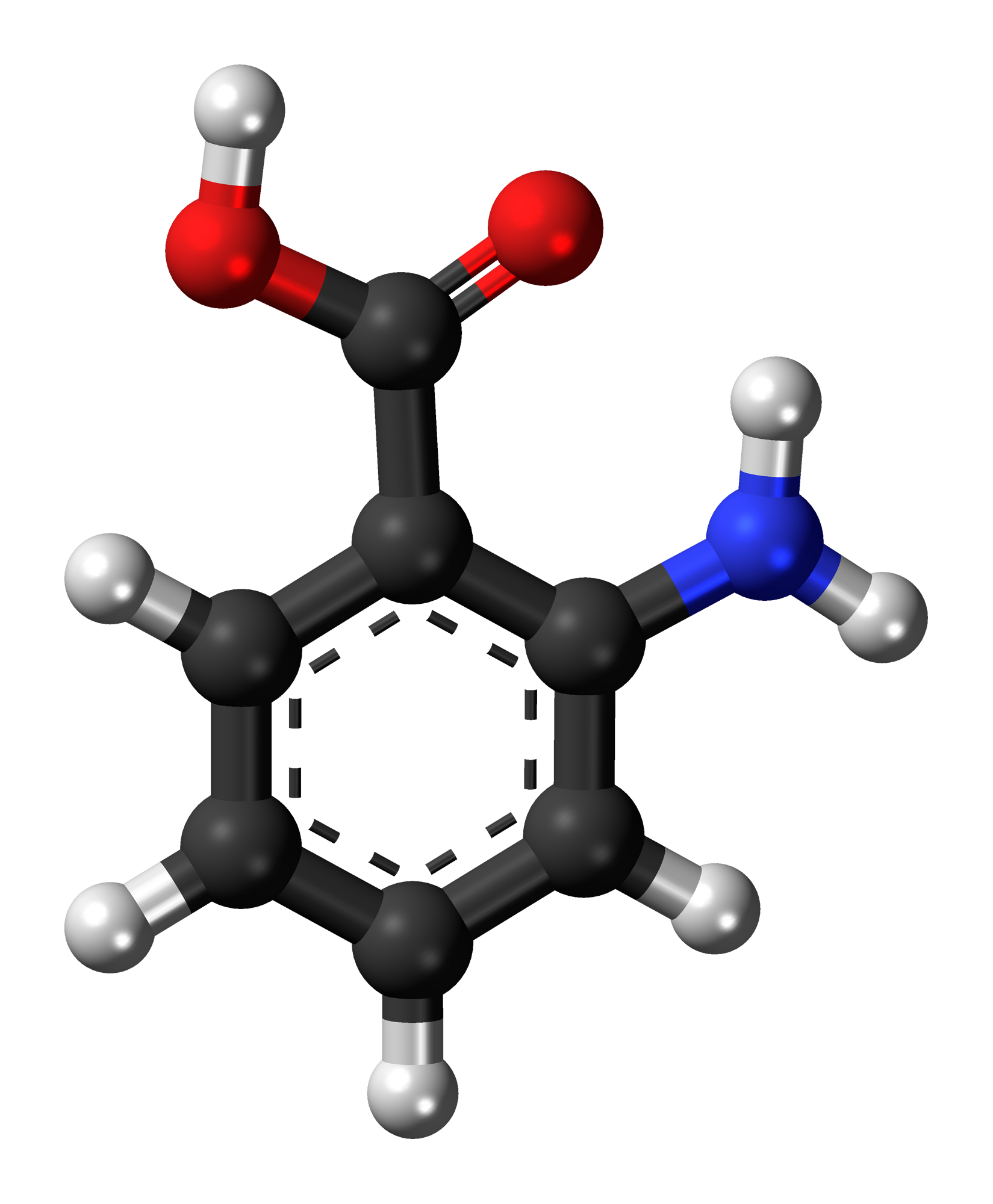
Observaciones: El ácido antranílico se emplea para la
síntesis del ácido N-acetilantranílico, que a su vez es la materia prima para
la producción clandestina de la metacualona y meclocualona. Ciertos ésteres del
ácido antranílico, por ejemplo, la pindocaína, están ahora fiscalizados
conforme a la CSA.
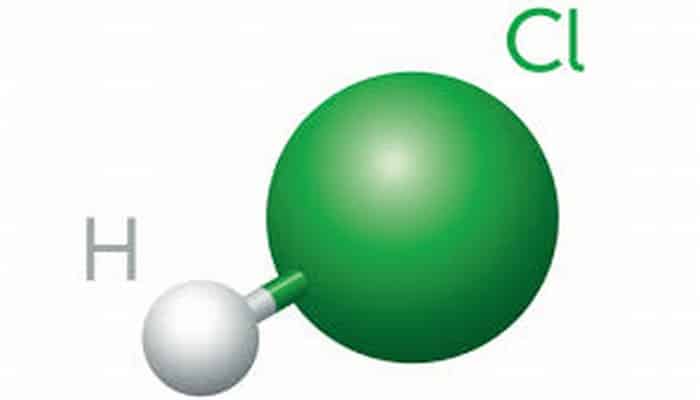
Usos ilícitos: En la obtención de clorhidratos de algunas
sustancias fiscalizadas que se producen clandestinamente, entre ellas, la
cocaína.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, Austria,
Bélgica, España, Finlandia, Francia, Grecia, Irlanda, Italia, Noruega, Países
Bajos, Portugal, Reino Unido, Suecia, Suiza. Asia: Corea del Sur, Filipinas, Indonesia, Japón,
Malasia, Singapur, Tailandia, Taiwán.
América Central: México. América del Sur: Bolivia, Colombia.
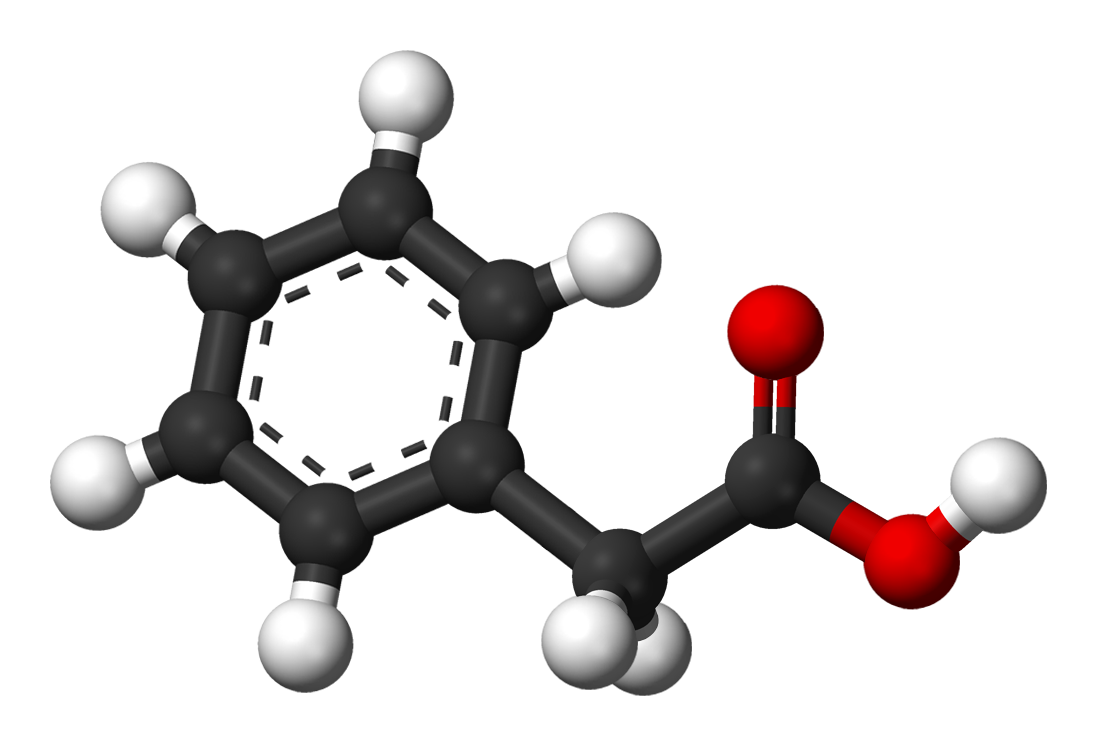
Usos lícitos: Fabricación de perfumes , ésteres
fenilacéticos, herbicidas, penicilina y diversos fármacos, aromatizante de
bebidas y alimentos edulcorantes.
ACIDO
FORMICO
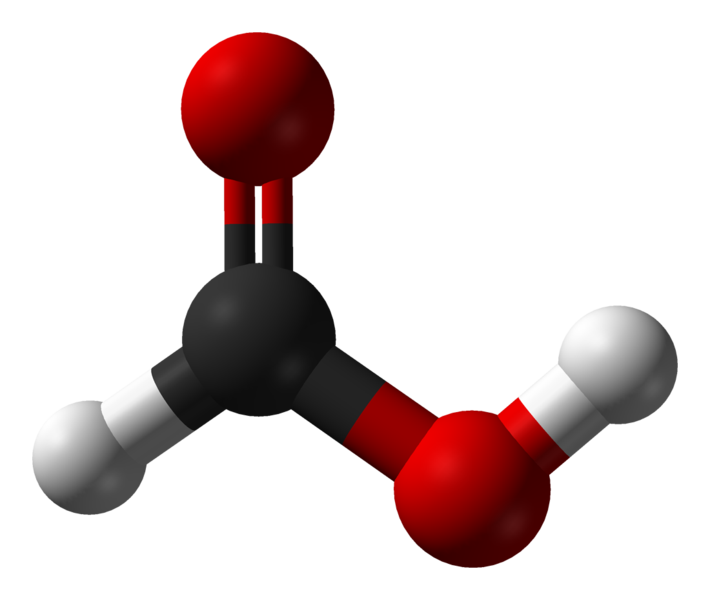
Otros nombres: Acido metanoico; ácido hidrógeno carbixílico, ácido amínico.
Fórmula molecular: HCOOH
Peso molecular: 46,02 (CH2O2)
Código armonizado: 2915.11.0000
Densidad: 1,22
Punto de ebullicion: 100,5¼C
Punto de congelación: 8,3¼C
Propiedades: Líquido incoloro de olor penetrante; poderoso agente reductor.
Peligros: El vapor irrita el sistema respiratorio y los ojos; el líquido quema los ojos y la piel; la ingestión causa irritación y lesiones internas serias; la absorción crónica provoca albuminuria y hematuria.
Usos ilícitos: En la producción de anfetamina y MDA.
Fiscalización: Se desconoce.
Usos lícitos: Agente desencalados; agente reductor en el teñido indeleble de la lana; en curtidos, en la depilación e hinchamiento de los pellejos; en galvanizado; en la coagulación del látex natural, en la regeneración del caucho usado; en análisis químico.
Obtención: Por reacción entre el monóxido de carbono y el hidróxido de sodio, al calor y bajo presión; el formiato de sodio resultante se descompone por medio del ácido sulfúrico.
ACIDO LISERGICO
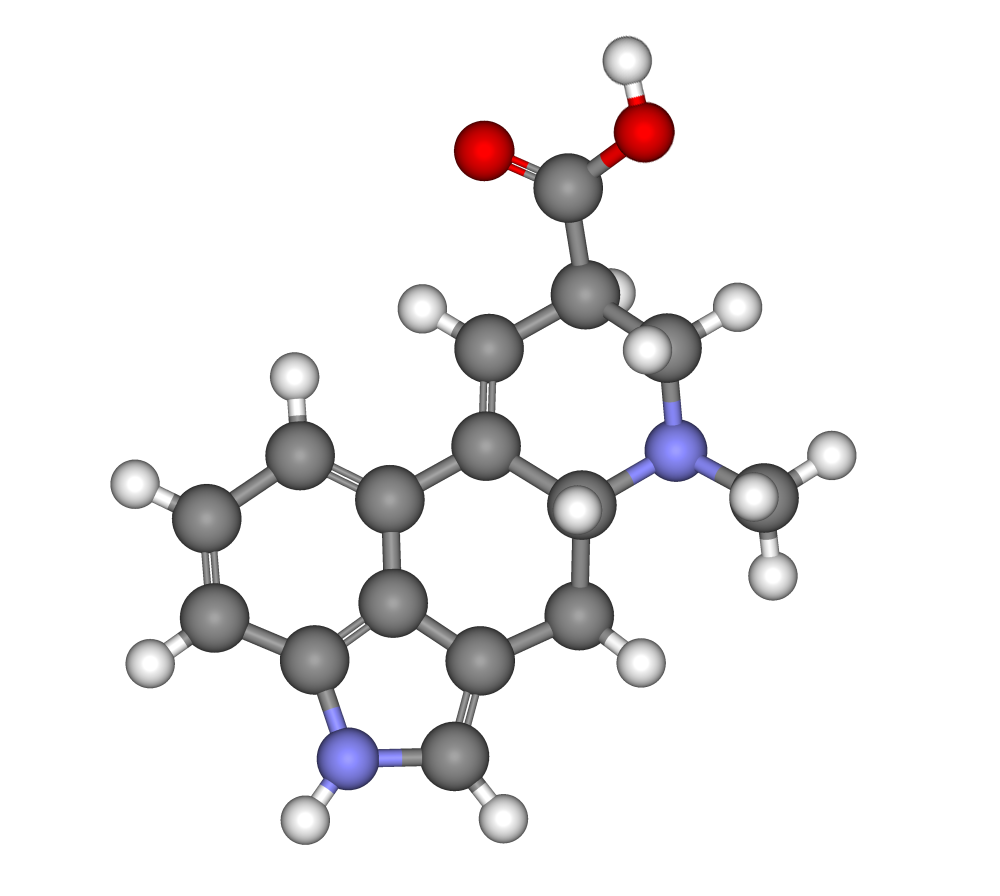
Otros nombres: Acido
9,10-dideshidro-6-metilergolín-8-carboxílico; ácido hexahidro-7-metilindolquinoleín-9-
carboxílico.
Fórmula Empírica: C16H16N2O2
Peso molecular: 268,32
Código armonizado: 2939.60.0000
Punto de fusión: 240¼C (con descomposición)
Propiedades: Material cristalino, poco soluble en agua y
en disolventes orgánicos neutros.
Usos ilícitos: En la síntesis del LSD (N,N-dietilisergamida,
o sea, la dietilamida del ácido d-lisérgico).
Fiscalización: CSA (sustancia fiscalizada de la lista III,
Estados Unidos); Organización de Estados Americanos (OEA); Naciones
Unidas. (Retirada de las listas de
sustancias químicas de la CSA a partir del 16 de abril de 1994).
Usos lícitos: En síntesis orgánica y de ergonivina; investigaciones médicas.
Obtención: Por hidrólisis alcalina de los alcaloides del
cornezuelo, como la ergotamina o ergonovina.
Por fermentación de cultivos de Claviceps purpurea o de Aspergillus
clavatus.
Transporte y almacenamiento: Se guarda en recipientes herméticos en
lugares frescos, protegido de la luz.
Observaciones: El ácido lisérgico es la materia prima
principal en dos métodos (al menos) de síntesis del LSD; a menudo se obtienea
partir del cornezuelo de centeno o de sus alcaloides. Aparece en los catálogos
de varios proveedores reactivos, tanto japoneses como estadounidenses.
ACIDO
SULFURICO
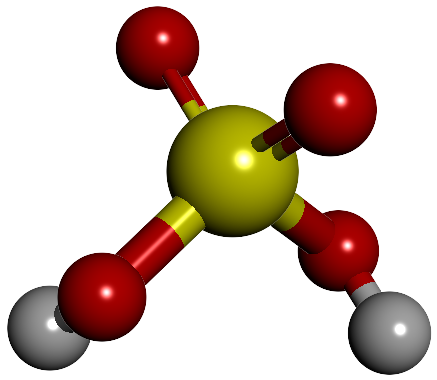
Otros nombres: Aceite de vitriolo, sulfato de hidrógeno.
Fórmula molecular: H2SO4
Peso molecular: 98,08
Código de la CSA: 6552
Código armonizado: 2807.00.0000
El ácido sulfúrico concentrado al 98%
presenta las siguientes constantes:
Punto de ebullición: 330¼C
Punto de congelación: 3¼C
Densidad: 1,84
Propiedades: Líquido aceitoso, transparente, incoloro e
inodoro, bastante más viscoso que el agua.
El ácido sulfúrico concentrado es una solución acuosa cuyo contenido de H2SO4 varía entre el
93 y 98%.
Peligros: El ácido sulfúrico concentrado corroe la piel
y quema los tejidos vorazmente. Cuando
se mezcla con otros líquidos , debe añadirse lentamente, con agitación
constante; si se diluye, añádase siempre el agua y nunca viceversa; reacciona
con el agua o vapor con generación de calor.
Usos ilícitos: Se usan soluciones diluidas (al 5-10%) en la
extracción de la cocaína de las hojas de coca, y en la conversión de la pasta
de coca en cocaína básica. También se emplea
en la formación de los sulfatos de diversas sustancias fiscalizadas.
Fiscalización: CSA; Organización de Estados Americanos
(OEA), Naciones Unidas.
Usos lícitos: En la fabricación de abonos, explosivos,
tintes, otros ácidos, papel y cola; en la purificación del petróleo; en la
oxidación de metales y otros materiales; como secante. Ingrediente de los
detergentes para baños, limpiadores de cañerías y metales, compuestos
antioxidantes, y fluidos de los acumuladores de automóviles.
Obtención: Por oxidación catalítica del dióxido de
azufre en trióxido de azufre, que a su vez se convierte en ácido sulfúrico por
el �método de contactoÓ (reacción con el agua). Por reacción entre el dióxido de azufre,
oxígeno, vapor de agua y óxidos de
nitrógeno en cámaras de plomo.
Transporte y almacenamiento: Sustancia corrosiva. Se transporta en garrafas de vidrio metidas
en cajas; cubetas portátiles de acero; camiones y vagones cisterna, y en
barriles y bidones de metal, según la concentración del ácido sulfúrico. Se guarda en recipientes herméticos de vidrio
u otro material inerte.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, Austria,
Bélgica, Dinamarca, España, Finlandia, Francia, Grecia, Italia, Noruega, Países
Bajos, Portugal, Reino Unido, Suecia, Suiza.
Asia: Corea del Sur, Indonesia,
Japón, Tailandia, Taiwán. América del
Sur: Colombia, Bolivia, Perú. Cercano Oriente: Siria.
Observaciones: Es la sustancia química que se produce en mayor cantidad en el mundo
(inclusive en los Estados Unidos). La
exportación estadounidense es baja con proporción a la producción. Es esencial disponer de un ácido para la
elaboración de la cocaína (producción de pasta de coca y de cocaína básica). Se pueden usar otros ácidos (nítrico, clorhídrico,
fosfórico) pero el preferido es el sulfúrico.
Cada vez es más común en América del Sur que los alcaloides de la
cocaína se extraigan de las hojas de coca mediante el uso de menores cantidades
de disolventes orgánicos (generalmente, el queroseno) de lo que se
acostumbraba. En su lugar, se maceran
las hojas de coca en ácido sulfúrico diluido, a fin de convertir los alcaloides
de la cocaína en sulfatos solubles en agua; estos se alcalinizan y extraen con
queroseno.
ACIDO
TARTARICO
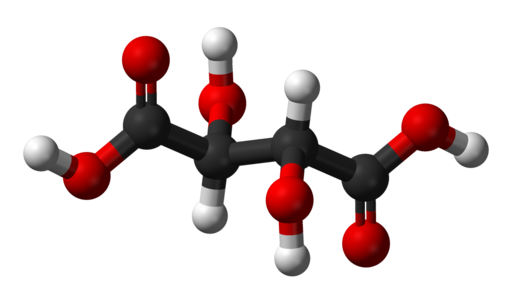
Otros nombres: Acido dihidroxisuccínico, ácido
2,3-dihidroxibutanodioico.
Fórmula molecular: (COOH)(OH)HCCH(OH)(COOH)
Peso molecular: 150,09 (C4H6O6)
Código armonizado: 2918.12.0000
Punto de fusión: 167-169¼C (dextro- y levo-tártarico); 206¼C
(racémico); 140¼C (meso-tartárico).
Propiedades: Cristales transparentes o polvo cristalino
blanco, de fino a granular; inodoro; fuerte sabor ácido. Se presenta en cuatro formas (isómeros
ópticos): dextro-tartárico, levo-tartárico, meso-tartárico y tartárico
racémico.
Peligros: Moderadamente tóxico por vía intravenosa;
ligeramente tóxico por ingestión oral.
Usos ilícitos: En la purificación de la morfina básica antes
de su conversión en heroína; en la preparación de tartratos de heroína y de
otras sustancias.
Usos lícitos: En la elaboración de gaseosas, dulces, pan,
postres de gelatina; en fotografía, curtiduría y alfarería; en la preparación
de tartratos; en productos farmacéuticos, como
Obtención: El ácido levo-tartárico se presenta
naturalmente en muchas frutas, se deposita en forma de la sal de potasio en la
fermentación de la uva. El ácido
tartárico seprepara a partir de esa sal, por neutralización con carbonato de
calcio y tratamiento posterior con ácido sulfúrico.
Transporte y almacenamiento: Sustancia considerada inocua que se reparte
en bidones y sacos de 22,5 y 45 kg (50 y 100 libras, respectivamente).
Fabricantes: Europa Occidental: Alemania, España, Francia, Italia, Suiza.
Asia: Japón.
Observaciones: El ácido tartárico se ha hallado en algunos
laboratorios de elaboración de la heroína, donde no es indispensable pero sirve
para aumentar la pureza del producto final.
ACIDO
YODHIDRICO

Otro nombres: Yoduro de hidrógeno en solución acuosa.
Fórmula molecular: HI
Peso molecular: 127,91
Código armonizado: 2811.19.6050
Densidad: 1,5 (al 47%); 1,7 (al 57%)
Punto de ebullición: 127¼C (al 57%)
Propiedades: Líquido corrosivo; es incoloro cuando está
recién preparado pero al exponerse a la luz y al aire se vuelve amarillento y
pardusco. Consiste en una solución de
yoduro de hidrógeno gaseoso en agua; se produce comercialmente en varias
concentraciones, entre ellas, al 47 y al 57% de HI.
Peligros: El vapor irrita el sistema respiratorio, la
piel y los ojos; el líquido causa quemaduras graves de los ojos y la piel; la
ingestión causa irritación interna y lesiones graves.
Usos ilícitos: Reductor en la preparación clandestina de la
metanfetamina a partir de la efedrina o seudofedrina.
Usos lícitos: Síntesis de compuestos orgánicos e
inorgánicos del yodo; desinfectante; en química como reactivo; en farmacia,
como suplemento (jarabe de ácido yodhídrico) de las dietas deficientes en yodo.
Obtención: Por reacción de los gases de yodo e hidrógeno
en presencia de un catalizador, y posterior absorción en agua. Por tratamiento del yodo con ácido
sulfhídrico en solución acuosa. Por reacción del yodo con fósforo rojo y agua.
Transporte y almacenamiento: Guárdese al abrigo del aire y de la luz, a
temperaturas inferiores a 30¼C.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania.
Asia: Japón.
Observaciones: El ácido yodhídrico es el reductor que más se
usa en la síntesis de la metanfetamina, pero hay sustitutivos. En los laboratorios clandestinos es cada vez
más corriente que se prepare el ácido yodhídrico por reacción a partir de
fósforo rojo, yodo y agua.
ALCOHOL
BUTILICO NORMAL
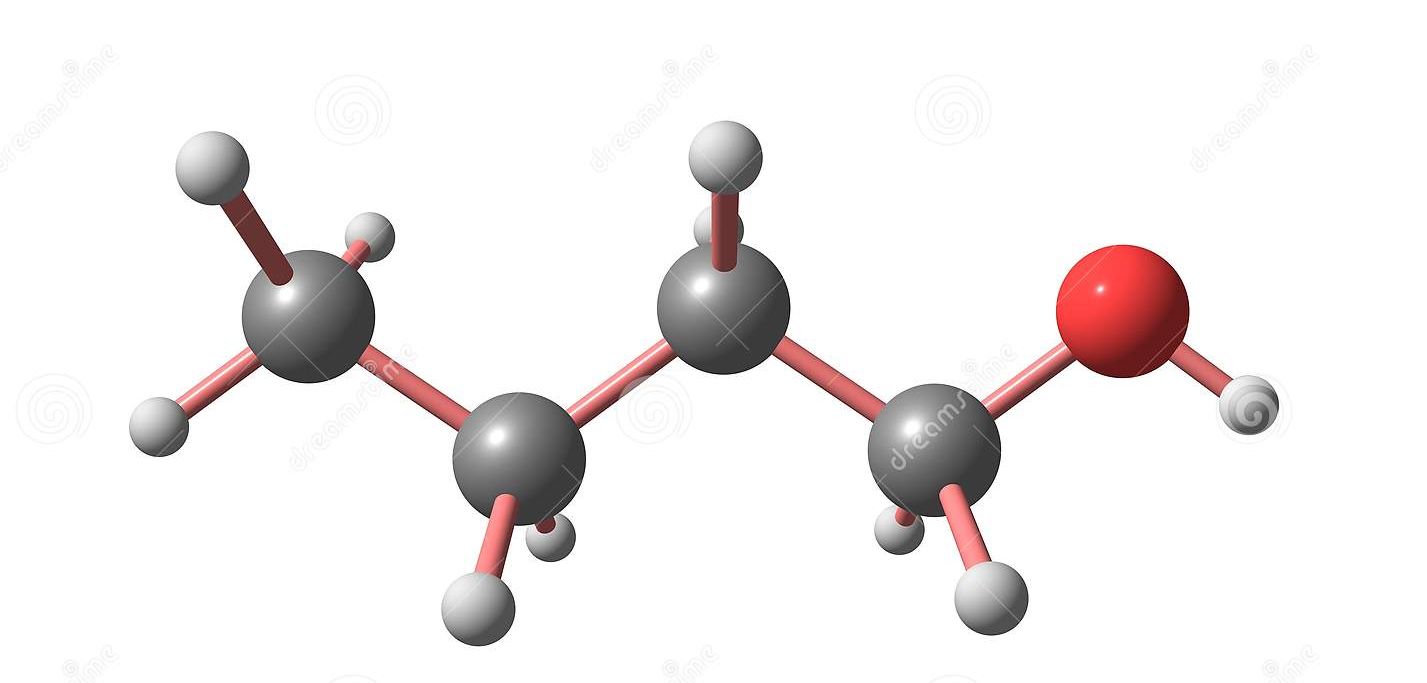
Otros nombres: Alcohol butílico; 1-butanol; n-butanol;
hidróxido butílico; 1-hidroxibutano; n-propilcarbinol.
Fórmula molecular: CH3(CH2)3OH
Peso molecular: 74,12 (C4H10O)
Código armonizado: 2905.13.0000
Densidad: 0,81
Punto de ebullición: 117-118¼C
Propiedades: Líquido incoloro de vapor irritante.
Peligros: Tóxico por contacto con la piel, por
ingestión y por vía subcutánea; irrita seriamente los ojos y la piel.
Usos ilícitos: disolvente de la cocaína básica y del ácido
clorhídrico en la conversión de la cocaína básica en clorhidrato de cocaína.
Usos lícitos: disolvente de grasas, ceras, resinas, gomas
laca, barnices y gomas; se usa en la fabricación de lacas, rayón y detergentes.
Obtención: Por hidrogenación del butiraldehido normal;
por reducción del butiraldehido normal con borohidruro de sodio.
Transporte y almacenamiento: En bidones de acero dulce sin tratar, de
acero esmaltado o, a veces, de acero inoxidable.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania,
España, Francia, Reino Unido, Suecia.
Asia: Corea del Sur, Japón.
Observaciones: Aunque esta sustancia no se ha encontrado en
el clorhidrato de cocaína confiscado en los Estados Unidos otra muy parecida,
el alcohol isobutílico, se halla con frecuencia.
ALCOHOL
BUTILICO SECUNDARIO
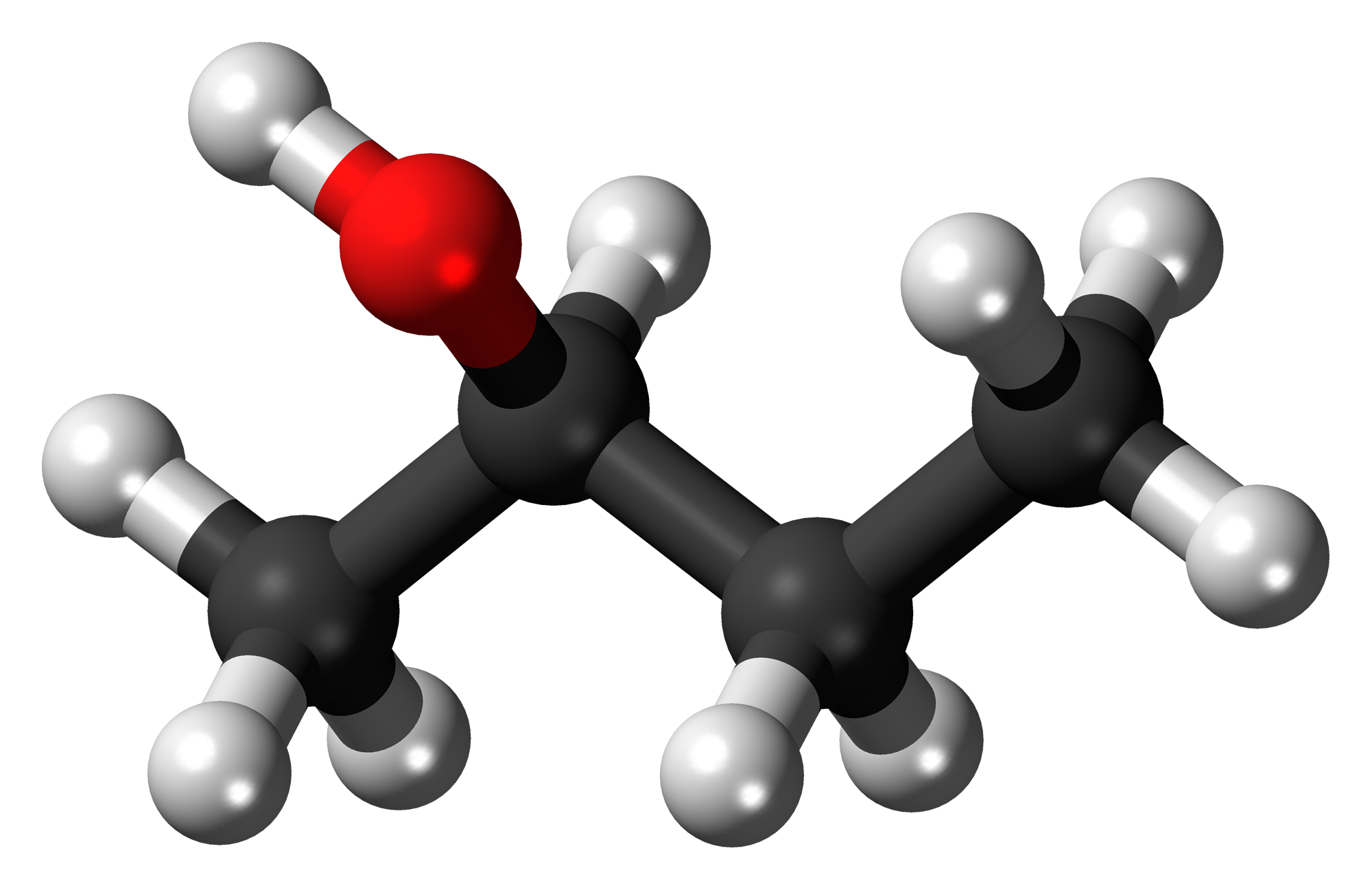
Otros nombres: 2-butanol; 2-hidroxibutano;
metiletilcarbinol.
Fórmula:
CH3CH2CH(OH)CH3
Peso molecular: 74,12 (C4H10O)
Código armonizado: 2905.13.0000
Densidad: 0,80
Punto de ebullición: 98-99,5¼C
Propiedades: Líquido incoloro de vapor irritante.
Peligros: Inflamable; el vapor irrita el sistema
respiratorio y los ojos; el líquido irrita los ojos y, a veces, la piel; la
ingestión causa dolor de cabeza, mareo, modorra y narcosis.
Usos ilícitos: disolvente de la cocaína básica y del ácido
clorhídrido en la conversión de la cocaína básica en clorhidrato de cocaína.
Usos lícitos: Síntesis de la metiletilcetona; preparación
de agentes de flotación, sabores, perfumes, tintes, humectantes; fabricación de
detergentes industriales y de quitapinturas; disolvente de resinas naturales y de
aceites de linaza y ricino.
Obtención: Por hidratación del 2-buteno
Transporte y almacenamiento: En bidones de acero dulce sin tratar, de
acero esmaltado o, a veces, de acero inoxidable.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, Francia, Países Bajos, Reino
Unido. Asia: Japón, Taiwán.
Observaciones: El 95%, aproxidamente, del alcohol butílico
secundario producido en los Estados Unidos se usa para la obtención de la metiletilcetona
por deshidrogenación; el 5% se emplea en disolventes y en la obtención de
sustancias químicas intermedias. Se ha
encontrado en muestras de clorhidrato de cocaína confiscadas en los Estados
Unidos.
ALCOHOL
ETILICO
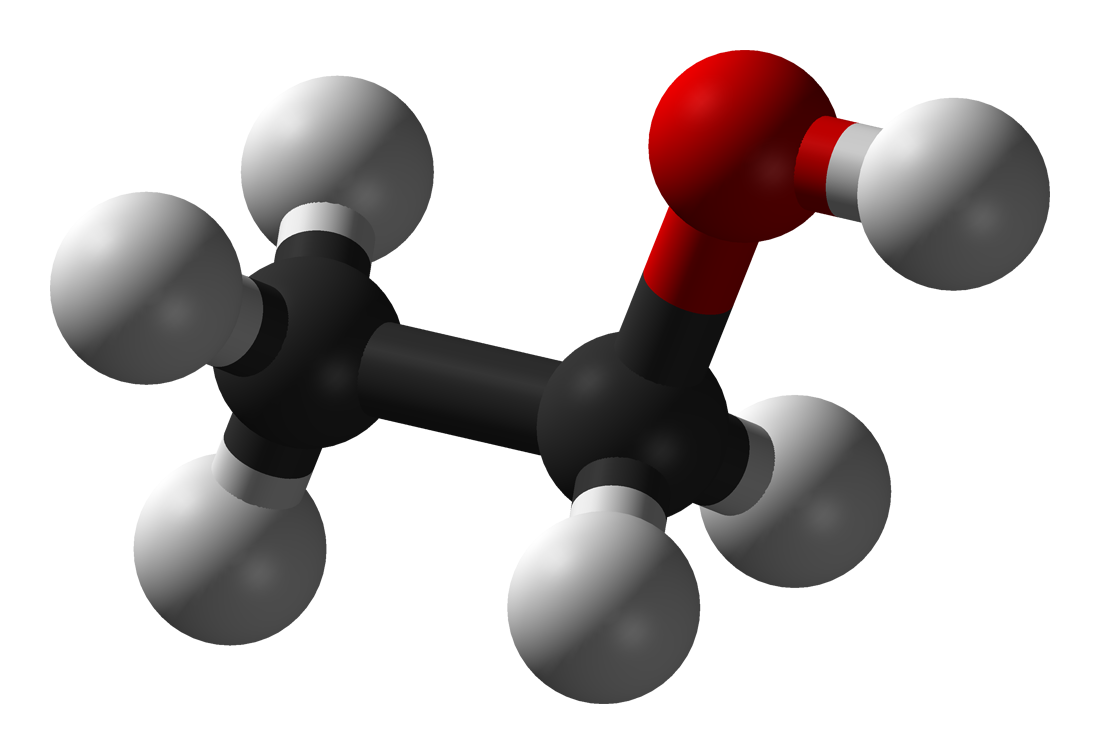
Otros nombres: Etanol; alcohol; alcohol anhidro; hidróxido
de etilo, metilcarbinol.
Fórmula molecular: CH3CH2OH (También, C2H5OH)
Peso molecular: 46,07 (C2H6O)
Código armonizado: 2207.10.6000 / 2207.20.0000
Densidad: 0,79
Punto de ebullición: 78,5¼C
Propiedades: Líquido incoloro, transparente e inflamable,
de olor agradable.
Usos ilícitos: disolvente que se emplea en la conversión de la
cocaína básica en clorhidrato de cocaína.
Peligros: Sumamente inflamable; ingerido en cantidades
importantes afecta a la percepción y la coordinación.
Fiscalización: Organización de Estados Americanos (OEA).
Usos lícitos: Bebidas alcohólicas, disolvente industrial;
aditivo antidetonante de la gasolina; en perfumería, síntesis orgánica, y la
elaboración de productos farmacéuticos.
Obtención: Por fermentación de almidón, azúcar y otros
hidratos de carbono. Por hidratación del
etileno.
Transporte y almacenamiento: Vagones y camiones cisterna; bidones y
recipientes más pequeños de vidrio o de metal; en ciertos casos, los bidones
van forrados de resina fenólica.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, Francia, Paises Bajos, Reino Unido.
Asia: Japón, Taiwán.
Observaciones: El 95%, aproximadamente, del alcohol butílico
secundario producido en los Estados Unidos se usa para la obtención de la
metiletilcetona por deshidrogenación; el 5% se emplea en disolventes y en la
obtención de sustancias químicas intermedias.
El alcohol butílico secundario se ha encontrado en muestras de
clorhidrato de cocaína confiscadas en los Estados Unidos.
ANHIDRIDO
PROPIONICO
Otros nombres: Anhídrido del ácido propiónico, Anhídrido
propanoico, anhídrido metilacético.
Fórmula molecular: (CH3CH2CO)2O
Peso molecular: 130,14 (C6H10O3)
Código de CSA: 8320
Código armonizado: 2915.90.5000
Densidad: 1,01
Punto de ebullición: 167¼C
Propiedades: Líquido incoloro y tóxico de olor picante;
soluble en alcohol, éter y cloroformo; insoluble en agua; combustible.
Peligros: Moderadamente tóxico si se ingiere; levemente
tóxico en contacto con la piel; irritante corrosivo para la piel, los ojos y
las membranas mucosas.
Usos ilícitos: En la preparación de fentanil y sustancias
análogas.
Usos lícitos: Esterificante de la celulosa, los aceites de
perfumería, las grasas y sobre todo, de la celulosa; en la producción de
resinas alquídicas, tintes y fármacos; deshidratante en reacciones de
sulfonación y nitración.
Obtención: Por deshidratación del ácido propiónico. Por carbonilación de ésteres del ácido
propiónico. Por oxidación catalítica del
propanal. A partir del monóxido de
carbono y el etanol.
Transporte y almacenamiento: En recipientes oscuros, secos y cerrados
herméticamente, para prevenir la descomposición que causa la humedad; en
vagones cisterna.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania.
Asia: Japón.
Observaciones: El anhídrido propiónico es uno de los
precursores que se usan en la síntesis del fentanil, la meperidina y sustancias
análogas.
BENCENO
Otros nombres: Benzol; ciclohexanotrieno.
Fórmula molecular: C6H6 [ cíclica]
Peso molecular: 78,11
Códigos armonizados: 2902.20.0000
(>90%) / 2707.10.0120 (<90%)
Densidad: 0,88
Punto de ebullición: 80,1¼C
Propiedades: Líquido transparente, incoloro y sumamente
inflamable.
Peligros: El vapor causa mareo, dolor de cabeza,
excitación y en concentraciones elevadas, desvanecimiento. El vapor irrita los ojos y las membranas
mucosas; el líquido es venenoso sise absorbe por la piel o se ingiere; la
inhalación frecuente en baja concentración puede ser causa de enfermedades
graves de la sangre, por ejemplo, de leucemia o anemia aplástica; se sospecha
que es carcinógeno.
Usos ilícitos: disolvente empleado en la conversión de la
cocaína básica en clorhidrato de cocaína; así como en la elaboración de la
feniciclidina.
Fiscalización: Organización de Estados Americanos (OEA).
Usos lícitos: disolvente de ceras, resinas y aceites;
preparación de etilbenceno, cumeno y ciclohexano; fabricación de barnices y
lacas; ingrediente de ciertos combustibles de motores.
Obtención: Por descomposición térmica de la nafta a
presión, en presencia de catalizador de platino. Por hidrogenación (con separación del azufre)
de la gasolina de pirólisis (a su vez, subproducto de la obtención del
etileno). En pequeña escala, por
coquización del carbón. Por
hidrodesalquilación y transalquilación del tolueno.
Transporte y almacenamiento: En bidones y cisternas de acero, previstos de
la debida ventilación.
Fabricantes: América del Norte: Estados Unidos. Europa:
Alemania, Austria, Bélgica, España, Finlandia, Francia, Italia, Países Bajos, Portugal, Reino Unido. Asia:
Corea del Sur, Indonesia, Japón, Singapur, Taiwán. América Central: México.
Observaciones: El benceno se puede usar para la extracción
inicial de los alcaloides de la hoja de
coca, pero no es la sustancia idónea, por su inflamabilidad y toxicidad
elevadas. Se encuentra algunas veces en
muestras confiscadas de cocaína, pero no está claro cuando se usa como tal en
la elaboración de la cocaína y cuando es sólo una impureza del didisolvente
principal.
ALCOHOL
ISOBUTILICO
 >
>
Otros nombres: Isobutanol; 2-metil-1-propanol;
isopropilcarbinol; 1-hidroximetilpropano.
Fórmula molecular: (CH3)2CHCH2OH, también (C4H9OH)
Peso molecular: 74,12 (C4H10O)
Densidad: 0,81
Punto de ebullición: 108¼C
Código armonizado: 2905.14.5010
Peligros: Es inflamable; el vapor irrita el sistema
respiratorio, y en concentraciones elevadas tiene efectos narcóticos; el
líquido irrita los ojos y resulta perjudicial si se ingiere.
Usos ilícitos: disolvente de posible uso en la conversión de
la cocaína básica en clorhidrato de cocaína.
Usos lícitos: En la síntesis de ésteres para preparar
aromas sintéticos de frutas; como disolvente en la fabricación de quitapinturas y
quitabarnices.
Obtención: Por extracción del aceite de fusel. Por fermentación de hidratos de carbono. Por hidrogenación del aldehido isobutírico. Como subproducto en la síntesis del metanol.
Transporte y almacenamiento: Botellas y bidones de polietileno.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, España, Francia,
Reino Unido. Asia: Corea del Sur, Japón.
Observaciones: En la preparación del clorhidrato de cocaína
se usa para disolver el ácido clorhídrico.
No es indispensable en ese procedimiento porque lo pueden sustituir
otros alcoholes. Se ha hallado en
muestras del clorhidrato de cocaína confiscadas en los Estados Unidos.
ALCOHOL
ISOPROPILICO
Otros nombres: 2-propanol; isopropanol; dimetilcarbinol;
petrohol; IPA.
Fórmula molecular: (CH3)2CHOH, también C3H7OH
Peso molecular: 60,09 (C3H8O)
Código armonizado: 2905.12.0050
Densidad: 0,78
Punto de ebullición: 82,5¼C
Propiedades: Líquido incoloro, de sabor ligeramente
amargo.
Peligros: Es inflamable; la inhalación del vapor en
altas concentraciones y la ingestión del líquido producen dolor de cabeza,
mareo, depresión mental, náusea, vómito, narcosis, insensibilidad y coma, el
líquido afecta gravemente los ojos.
Usos ilícitos: Para la recristalización de los clorhidratos
de ciertas sustancias fiscalizadas producidas clandestinamente; como disolvente
en la conversión de la cocaína básica en clorhidrato de cocaína.
Usos lícitos: disolvente, extractador, deshidratante,
descongelante y desinfectante. Se emplea
como materia prima en la producción de acetona y de otros compuestos. El alcohol isopropílico de primera calidad se
usa para componer productos higiénicos, como, cremas para la piel, preparados
para el cabello y esmalte de uñas.
Obtención: Por oxidación del propileno con ácido
sulfúrico. Por hidrogenación de la
acetona.
Transporte y almacenamiento: Frascos y bidones de polietileno; cubetas
metálicas.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, España, Francia, Paises Bajos,
Reino Unido. Asia: Corea del Sur,
Japón, Singapur, Taiwán. América
Central: México. América del Sur: Argentina, Brasil, Perú, Venezuela.
Observaciones: El alcohol isopropílico sirve para
solubilizar el ácido clorhídrico en los disolventes que se emplean en la elaboracion del clorhidrato de cocaína
; en esa función se puede sustituir por otros alcoholes, como el metílico,
etílico o isobutílico. Este disolvente, en
combinación con otros, se ha hallado en muestras líquidas obtenidas en América
del Sur y en clorhidrato de cocaína confiscado en los Estados Unidos. Sirve de materia prima en la producción de
acetona.
ALCOHOL
METILICO
Otros nombres: Metanol; carbinol, alcohol de madera.
Fórmula molecular: CH3OH
Peso molecular: 32,04 (CH4O)
Código armonizado: 2905.11.1000 / 2905.11.2000
Densidad: 0,79
Punto de ebullición: 64,7¼C
Propiedades: Líquido movedizo, transparente e incoloro; al
arder produce una llama azulada.
Peligros: Es inflamable; la inhalación del vapor en
altas concentraciones causa mareo, estupor, calambres y trastornos digestivos;
en concentraciones inferiores, causa dolores de cabeza, náusea, vómito e
irritación de las membranas mucosas; el vapor y el líquido son sumamente
peligrosos para los ojos; la ingestión afecta al sistema nervioso central,
especialmente el nervio óptico y causa ceguera temporal o permanente; la
ingestión también afecta a los riñones, el hígado y el corazón, entre otros
órganos; produce la pérdida del conocimiento a las pocas horas, y a veces,
provoca seguidamente la muerte.
Usos ilícitos: En la recristalización de los clorhidratos de
algunas sustancias fiscalizadas de producción clandestina; disolvente en la
conversión de la cocaína básica en el clorhidrato.
Usos lícitos: disolvente industrial; anticongelante; aditivo
antidetonante de la gasolina; para la desnaturalización del alcohol etílico
(etanol); materia prima para la producción de formaldehido y de los ésteres
metílicos de los ácidos orgánicos e inorgánicos; disolvente de uso farmaceútico.
Obtención: Por destilación al vacío de la madera. Por reducción catalítica del monóxido de carbono
(o del dióxido) por el hidrógeno. Por
oxidación de hidrocarburos. Asimismo, es subproducto de la producción del
tereftalato de polietileno , cuando se usa como materia prima en el tereftalato
de dimetilo.
Transporte y almacenamiento: En recipientes herméticos, alejados del
calor, las chispas y las llamas abiertas.
Fabricantes: América del Norte: Estados Unidos. Europa: Alemania, Grecia,
Italia, Países Bajos, Reino Unido,Suiza, Rusia.
Asia: Indonesia, Japón, Malasia,
Tailandia, Taiwán. América del Sur:
Argentina, Brasil, Colombia, Chile, Venezuela. América Central: México.
Observaciones: Se usa para disolver el ácido clorhídrico, en
la preparación del clorhidrato de cocaína.
El metanol no es indespensable, puesto que en su lugar se pueden emplear
otros alcoholes, como el etílico, el isopropílico, etc. El metanol se emplea junto con disolventes insolubles en agua. Se ha hallado en muestras de clorhidrato de
cocaína.
ANHIDRIDO
ACETICO
Otros nombres: óxido acético; anhídrido del ácido acético,
óxido de acetilo; anhídrido etanoico.
Fórmula molecular: (CH3CO)2O
Peso molecular: 102,09 (C4H6O3)
Código de la CSA: 8519
Código armonizado: 2915.24.0000
Densidad: 1,08
Punto de ebullición: 139¼C
Propiedades: Líquido incoloro, de olor acético penetrante
y sofocante; es fumante en el aire húmedo.
Peligros: Es inflamable; los vapores son muy irritantes
para el sistema respiratorio y los ojos; el líquido quema gravemente los ojos y
la piel; la ingestión causa irritación, dolor y vómito.
Usos ilícitos: Como acetilante en la preparación de la
heroína, la fenilacetona y el ácido N-acetilantranílico.
Fiscalización: CSA, Naciones Unidas, Organizacion de Estados
Americanos (OEA).
Usos lícitos: En química, como agente acetilante y
deshidratante. Aproximadamente el 80% se
emplea en la acetilación de la celulosa.
También encuentra aplicación en la producción de poli(metilacrilimida)
(espuma dura), plastificantes acetilados, explosivos, ciertos fluidos para
frenos hidráulicos, fluidos de perforación, activadores para detergentes de
blanqueo al frío, tintes (principalmente junto con el ácido nítrico),
intermedios orgánicos, fármacos, alimentos(acetilación de grasas animales y
vegetales), herbicidas, aromas y fragancias.
Obtención: Por deshidratación del ácido acético. Por carbonilación del acetato de metilo.
Transporte y almacenamiento: En recipientes forrados de acero inoxidable o
polietileno.
Fabricantes: América del Norte: Estados Unidos. Europa Occidental: Alemania, Francia, Reino Unido, Suiza. Asia:
Japón. América Central: México.
América del Sur: Brasil.
Observaciones: La reacción del anhídrido acético con la
morfina produce heroína; con el ácido antranílico, ácido N-acetilantranílico
(precursor inmediato de la metacualona y la meclocualona); con el ácido
fenilacético, fenil-2-propanona (fenilacetona o P-2-P, precursora de la
metanfetamina y la anfetamina).
CONTINUARÁ...
© 2022 JAVIER DE LUCAS