
BIOMOLECULAS

Hasta finales del siglo XX un dogma científico de los biólogos moleculares era que la función o actividad biológica de las biomoléculas (moléculas de la vida como las proteínas, las enzimas, etc.) está basada en su estructura y se deriva de ella. En otras palabras, la estructura de estas moléculas y su actividad bioquímica están íntimamente relacionadas. Este dogma tuvo sus detractores como, por ejemplo, el físico ruso laureado con el Premio Nobel I. Prigogine, que pensaba justamente lo contrario, es decir, que es la función la que crea la estructura.
Las conocidas como proteínas dúctiles cambiaron esta forma de pensar, ya que no adoptan una estructura definida para realizar una función. En cualquier caso, la función y la estructura forman muy a menudo una pareja indisoluble: no se puede entender la una sin la otra. Es interesante resaltar que las propiedades que tienen ciertas asociaciones de moléculas no las muestran las moléculas que la constituyen. Eso también ocurre a nivel celular y en muchos sistemas complejos. La complejidad que surge en un sistema no puede entenderse generalmente a partir de sus componentes debido a la aparición de nuevas propiedades globales (propiedades emergentes). No lo olvidemos: «More is different». Este artículo está cargado inevitablemente de tecnicismos propios de la química cuántica y la biología molecular. Pido disculpas al lector, que se tiene que preparar para leer un capítulo un tanto árido, pero necesario para acercarse a los grandes interrogantes de la vida. Intentaré, en la medida de lo posible, ser claro y conciso, y no añadir más términos y conceptos químicos que los necesarios.
§. El enlace
El reduccionismo ha sido la manera más usual de entender y explicar la ciencia. Sabemos que un átomo está formado por electrones con cargas negativas que están orbitando alrededor de un núcleo formado por protones con cargas positivas y neutrones carentes de carga eléctrica. Cada una de estas partículas las consideraremos elementales a lo largo de este libro, a sabiendas de que los protones y neutrones están formados por quarks que se manifiestan en rangos de energías muy superiores a los que ocurren los procesos vitales. Los electrones que siguen ciertas órbitas (o capas) alrededor del núcleo constituyen menos del 0,06% de la masa del átomo. Una molécula es una asociación o unión de átomos dispuestos geométricamente en el espacio manteniéndose unidos mediante enlaces químicos. Con otras palabras, si una molécula se considera como un edificio o estructura, los átomos que la forman son sus ladrillos y los enlaces químicos son la argamasa que los mantiene unidos. Otra analogía: las moléculas serían como las figuras planas o tridimensionales que se construyen con las piezas de LEGO, que serían los átomos; los engranajes de las piezas serían los enlaces. Podríamos hablar de un LEGO químico y/o bioquímico.
El conocimiento de la estructura o edificio molecular es esencial para una mejor comprensión de la actividad o función de las moléculas, en particular, de las biomoléculas. La molécula es la unidad menor en que puede dividirse una sustancia química conservando sus propiedades características. Más aún, se sabe que las moléculas poseen nuevas e insospechadas propiedades que no muestran los átomos que la constituyen. Estas nuevas propiedades que emergen cuando se unen los átomos hace que ese reduccionismo, utilizado para entender el edificio molecular, no sea suficiente para lograr una total comprensión de la actividad de las moléculas cuando están inmersas en distintos medios como en fase gas, líquida o sólida. Por ejemplo, la molécula de agua, H2O, que está formada por dos átomos de hidrógeno (H) y un átomo de oxígeno (O), tiene propiedades notablemente diferentes a la de los átomos que la constituyen. Las moléculas de agua tienen comportamientos diferentes si se encuentran en estado líquido o en forma de hielo. Por tanto, a medida que las estructuras moleculares crecen en complejidad con la participación de un elevado número de átomos para formar superestructuras tridimensionales, nuevas y sorprendentes propiedades van emergiendo radicalmente diferentes a las propiedades de sus elementos constitutivos (igual que con las figuras creadas por las piezas de LEGO).
El caso de las biomoléculas (proteínas, lípidos, glúcidos o hidratos de carbono y ácidos nucleicos) es particularmente dramático porque además estamos hablando del paso de la materia inanimada a la animada. Los electrones de las capas más externas de los átomos que conforman una molécula participan en la formación del enlace químico. Al poder, potencialidad o capacidad de combinación de los átomos se le denomina la valencia, que nos dice la cantidad de electrones más externos que efectivamente participan en un enlace químico. Los espines de esos electrones también cumplen el principio de exclusión de Pauli. Si cada enlace está formado por dos electrones provenientes uno de cada átomo involucrado, estos tienen que tener espines antiparalelos. La mayoría de las moléculas son estables, no tienden a desintegrarse o descomponerse con el paso del tiempo. De hecho, se requiere bastante energía para romper las moléculas en los átomos que las integran. Esa energía varía de acuerdo a la fortaleza del enlace químico. Más aún, en la formación de una molécula estable se libera energía, ya que esta posee una energía más baja que la de los átomos que la forman.
A mi modo de ver, la manera más simple de entender este comportamiento energético es la siguiente: pensemos en un pantano situado en lo alto de una montaña, el agua está situada a una cierta altura y posee, como recordaremos de nuestros años en la enseñanza secundaria, energía potencial. Esta energía se manifiesta cuando se abren las compuertas para que el agua liberada caiga a un nivel más bajo (un valle), donde hay una turbina, provocando su giro para generar energía eléctrica. Lo mismo ocurre con una batería de móvil, de ordenador, etc.: la batería tiene energía potencial eléctrica, la que necesitará el artilugio para funcionar. Imaginemos ahora un esquema energético donde la altura significa más energía (cuando se está en lo alto de una montaña) y el valle representa un nivel de energía más bajo (la falda de la montaña). Los átomos que constituyen el agua, H y O, están en un estado energético alto que puede asimilarse a una energía potencial. Esa energía potencial se manifiesta cuando los átomos se unen para formar la molécula de agua, H2O, pasando esta a un estado energético más bajo (el valle) que el de sus componentes atómicos. Esta imagen quedará más clara cuando hablemos del esquema energético de una reacción química.
El estudio de la naturaleza del enlace químico es uno de los principales objetivos de la química cuántica. Aquí solo describiré cualitativamente los más importantes que tienen lugar dentro de la biología molecular. El llamado enlace iónico o electrovalente hace que dos iones atómicos de cargas opuestas (positiva y negativa) se atraigan a través de la fuerza electrostática según la ley de Coulomb. El ejemplo más típico es la sal común, cuya molécula está simbolizada químicamente por NaCl, formada por un átomo de cloro (Cl) y un átomo de sodio (Na). Esta molécula se forma porque los correspondientes iones atómicos Na+ (el signo + nos indica que el átomo de Na ha perdido un electrón de su última capa y queda cargado positivamente) y Cl− (el signo − nos indica que el átomo de Cl ha ganado un electrón en su última capa y queda cargado negativamente) permanecen juntos o unidos por la fuerza electrostática atractiva. El origen de esa ionización se debe a la descompensación de la carga total de electrones con la de los protones de los núcleos. En un átomo neutro (o no ionizado) hay el mismo número de electrones que protones.
Ahora, según la famosa ley de Coulomb: dos cargas de distinto signo se atraen, las del mismo signo se repelen. El enlace iónico (fuertemente atractivo) puede considerarse como un enlace «egoísta» ya que los iones permanecen unidos a expensas de que el Cl le «quita» un electrón al Na ya que el Cl tiene mucha «avidez» de electrones y el Na se lo deja quitar fácilmente. Se dice entonces que el Cl es un elemento muy electronegativo y el Na muy electropositivo. Los cristales de la sal común están formados por muchos iones de sodio y cloro unidos por el enlace iónico.
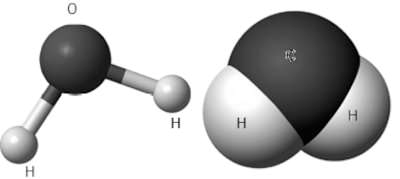
Figura 1. Dos representaciones de la molécula de agua, H2O. El ángulo que forman los dos enlaces covalentes O−H es de 104,45º y la longitud del enlace es de 95,84 pm (1 pico-metro (pm) = 10-12 metros).
En la molécula de ácido clorhídrico, HCl, los dos electrones del enlace pasan más tiempo cerca del Cl que del H, ya que el Cl es más electronegativo que el H. De esta forma, se crea una acumulación de carga negativa alrededor del Cl y un defecto de carga negativa (o carga positiva) alrededor del H. Entonces hablamos de que la molécula está polarizada o forma un dipolo. Un dipolo (eléctrico) es la asociación de una carga positiva y otra negativa próximas entre sí, a una distancia dada. Es parecido a un imán que tiene su polo positivo y negativo pero, en vez de hablar de campos eléctricos, hablamos de campos magnéticos.
En la molécula de agua, cada átomo de hidrógeno está unido al átomo de oxígeno formando un enlace covalente, mientras que entre ellos no están unidos. El enlace covalente se representa por un segmento de recta entre los átomos unidos. Así, la molécula de agua posee dos enlaces covalentes del tipo O-H. En cada enlace covalente hay también dos electrones, uno proviene del H y el otro del O. Este enlace es como una «pareja» donde los electrones se comparten más o menos al 50% y se consideran los dos electrones como «bienes gananciales». Como se aprecia en la figura 6, la molécula de agua no es lineal, ya que los dos enlaces covalentes forman un ángulo aproximado de 105º. Cuando se dice que en este enlace se «comparten» los electrones casi al 50% quiere decir que a veces hay muchas moléculas donde uno de los dos átomos atrae más a los electrones que el otro, dependiendo de su naturaleza electronegativa y/o electropositiva. El O es más electronegativo que el H y, por tanto, los electrones del enlace pasan más tiempo orbitando alrededor del O que del H, hablando también de la presencia de un dipolo eléctrico.
Hasta ahora hemos puesto ejemplos sencillos y bien conocidos de nuestros años de colegio de lo que se conoce como química inorgánica. En la química orgánica, los compuestos están formados principalmente por carbono (C), hidrógeno, oxígeno, nitrógeno (N) y, en menor medida, por fósforo (P) y azufre (S). En algunas ocasiones también hay elementos metálicos como hierro (Fe), níquel (Ni), cobre (Cu), etc., que es el caso de las metaloproteínas o muchas enzimas. Estas moléculas orgánicas son fundamentales para la biología y permanecen unidas principalmente mediante enlaces covalentes que pueden ser simples, dobles y triples. En la figura 7 presentamos las moléculas de etileno (C2H4), acetileno (C2H2), benceno (C6H6), ácido fórmico (CH2O2), acetona (C3H6O) y cianuro sódico (NaCN). La variedad de enlaces en las biomoléculas es amplísima con un predominio claro de los enlaces covalentes simples y dobles y una presencia exigua de los enlaces triples.
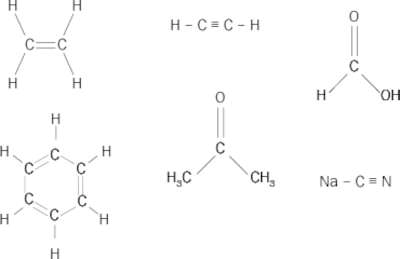
Figura 2 En la primera fila presentamos, de izquierda a derecha, algunas moléculas orgánicas cuyas fórmulas químicas corresponden al etileno, acetileno y ácido fórmico. En la segunda fila, análogamente, tenemos las moléculas de benceno, acetona y cianuro de sodio.
Es interesante observar que cuando una molécula posee, por ejemplo, un enlace doble, los electrones del segundo enlace covalente no se hallan alrededor de ningún átomo en particular, pertenecen a la molécula como un todo. Se llaman electrones no localizados y se denominan electrones π y su enlace, enlace π (de la letra griega pi). En el enlace triple, hay dos enlaces π. Cuando una molécula está formada por una cadena (abierta o cerrada) de átomos de C unidos por enlaces simples y dobles, hablamos de que la cadena está conjugada.
El caso más paradigmático es la molécula de benceno (C6H6) que posee una geometría hexagonal (plana) como muestra la figura 8. Las diferentes formas de representar el benceno se denominan estructuras de Kekulé debido a su descubridor A. Kekulé, primer químico orgánico alemán que intuyó esta estructura (a través de un sueño donde imaginó una serpiente mordiéndose la cola) a partir de evidencias experimentales acumuladas durante años. Cuantas más configuraciones puedan usarse para representar la molécula (configuraciones resonantes), más estable será la molécula, es decir, más energía hará falta para romperla. Se habla de configuraciones resonantes porque los electrones se encuentran muy deslocalizados a través de toda la molécula, por arriba y debajo del plano molecular.
Esta deslocalización electrónica es la base del almacenamiento de la energía en la célula. Uno de los ejemplos más conocidos en biología es la hidrólisis o reacción química de cualquier molécula con el agua, del ATP (trifosfato de adenosina) donde se libera una importante cantidad de energía. Las estructuras moleculares que hemos descrito hasta ahora son rígidas, consistentes y, en general, direccionales, ya que los enlaces forman ángulos (figura 1).
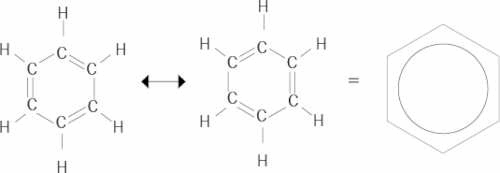
Figura 3. Las dos estructuras resonantes de Kekulé para la molécula de benceno (en el plano de la hoja de papel). Los electrones π están de hecho deslocalizados a lo largo del anillo hexagonal, por arriba y por abajo del plano molecular, es decir, de la hoja de papel. Ni la una ni la otra son buenas representaciones de la molécula, sino una combinación lineal (o superposición) entre ellas. Se acepta hoy en día que la mejor representación es un anillo bencénico y dentro un círculo que indica que los electrones π del doble enlace están orbitando por arriba y por abajo del plano.
Los enlaces tienen lugar dentro del edificio molecular y entonces se habla de enlaces intramoleculares. Por el contrario, también existen una serie de enlaces llamados intermoleculares, que son enlaces más débiles, y tienen lugar bajo la presencia de más de una molécula. Son muy importantes ya que juegan un papel esencial en la biología y, por tanto, en la vida. Las estructuras que se forman son más complejas, no direccionales y flexibles (poco rígidas). El enlace dipolo-dipolo se forma cuando moléculas polares (representadas por dipolos eléctricos permanentes) se acercan mucho entre sí, orientándose adecuadamente según el signo de las cargas (positiva con negativa y viceversa).
La molécula del ácido clorhídrico, por ejemplo, forma un dipolo permanente por la alta electronegatividad del Cl. Cada molécula de HCl se denomina monómero y cuando dos de estos monómeros se atraen, forman un dímero. Se atraen los dos monómeros orientándose de tal manera que el Cl de una molécula cargado negativamente se alinea con el H de la otra molécula que está cargado positivamente. Este enlace se representa por una línea discontinua como HCl---HCl o simplemente (HCl)2. Otro ejemplo es el dímero del fluoruro de sodio NaF---NaF donde F indica flúor. Si existieran muchas de estas moléculas o monómeros en un recipiente, se asociarían todas ellas formando un polímero (es decir, muchos monómeros) siguiendo el esquema del dímero del HCl o del NaF. El llamado enlace de hidrógeno, que es un tipo especial de enlace dipolo-dipolo, solo ocurre con la presencia del H.
El ejemplo más conocido es el que se da cuando dos o más moléculas de agua están muy próximas entre sí y el hidrógeno de una molécula se une al oxígeno de otra molécula de agua y así sucesivamente. Se representa generalmente como (H2O)n donde n es un número natural (n = 2, 3, 4…). Y, por último, está el enlace de Van der Waals, nombre que hace honor al laureado físico holandés J. D. van der Waals, que recibió el Premio Nobel en 1910. Los lagartos pueden adherirse a las paredes y techos debido precisamente a esta unión o fuerza atractiva. En este enlace, en vez de estar presentes dipolos permanentes, se tiene la interacción entre dipolos inducidos (no permanentes; es decir, que varían con el tiempo) cuando están muy cerca uno del otro. Si al enlace de Van der Waals le asignáramos una energía de enlace unidad (energía que hace falta suministrar para romper dicho enlace), el enlace de hidrógeno sería del orden de 4 veces mayor, el dipolo-dipolo de 5, el iónico estaría sobre 120, el covalente podría variar entre 60 y 110, y el enlace covalente doble entre 145 y 170, dependiendo siempre de los átomos involucrados. Cuanta más energía hace falta para romper los enlaces de una molécula, menores son las distancias de enlace entre los átomos que la forman y la molécula es más estable.
§. La reacción química
La reacción química es un proceso de transformación donde dos o más sustancias, llamadas reactivos, cambian sus estructuras moleculares mediante la rotura de sus enlaces para formar otras sustancias con diferentes estructuras moleculares y con nuevos enlaces, llamados productos. Se representa formalmente por la ecuación química siguiente:
A + B ←→ C + D
siendo las sustancias A y B los reactivos, y las sustancias C y D los productos. La doble flecha indica que, en principio, la reacción puede transcurrir en un doble sentido, es decir, es reversible. Las magnitudes conservadas son el número de átomos presentes, la carga eléctrica y la masa total. Una ecuación química, para estar correcta, tiene que estar ajustada como podemos recordar de nuestros años de enseñanza secundaria. Por ejemplo, la sal común (NaCl) se obtiene de la combinación de átomos Na y Cl según la reacción
2 Na (s) + Cl2 (g) ←→ 2 NaCl (s),
donde muchas veces se indica también el estado en que se encuentran las sustancias involucradas: estado sólido (s), líquido (l) o gas (g). Esta reacción se conoce como de combinación o síntesis, ya que se forma una nueva sustancia, la sal común, a partir de sus componentes. La reacción inversa se denomina de descomposición pues volvemos a recuperar sus componentes.
Hay muchas clases de reacciones químicas que se clasifican en diferentes categorías atendiendo a criterios de estructura, de energía y de intercambio de partículas. Esta clasificación es bastante flexible pues hay reacciones que podrían estar ubicadas en categorías diferentes al mismo tiempo. Si nos fijamos en el intercambio de energía, se puede hablar de reacciones exotérmicas y endotérmicas. La combustión es una buena ilustración de una reacción exotérmica y una de las más conocidas es la combustión del carbono según
C (s) + O2 (g) → CO2 (g) + calor.
Las reacciones endotérmicas necesitan el aporte de calor o energía para poderse llevar a cabo. También de nuestros años en la enseñanza secundaria, todos recordamos la famosa reacción química
ácido + base → sal + agua,
que puede ser ilustrada por
HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l),
que nos dice que el ácido clorhídrico (HCl) se combina con el hidróxido sódico (NaOH) para dar el cloruro de sodio (NaCl) y el agua (H2O) (aq significa que la sustancia está diluida en agua y la reacción ocurre en medio acuoso). En esta reacción se intercambian protones. Si se intercambian electrones, la reacción se denomina de oxidación-reducción o redox como en
2 NaI (s) + Cl2 (g) → I2 (g) + 2 NaCl (s),
donde el cloro molecular (Cl2) toma dos electrones del yoduro de sodio (NaI) para formar iodo molecular (I2) y cloruro sódico. Se dice entonces que el cloro se reduce al ganar electrones mientras el yodo (I) del yoduro de sodio se oxida al perder electrones para formar nuevos enlaces, los del iodo molecular (I2) y la sal común. La regla estándar aquí es: el elemento que se reduce se denomina oxidante y el que se oxida, reductor. En la reacción de la formación del agua, el O es el oxidante y el H el reductor. Estas reacciones redox son importantes en muchos ámbitos como en la corrosión, combustión, etc. No obstante, son especialmente importantes y fundamentales en el metabolismo de los seres vivos con la presencia de sustancias orgánicas, no de sustancias inorgánicas como acabamos de ilustrar con estas reacciones químicas.
Otra clase de reacciones muy importantes es la electrólisis en la cual se aporta energía por medio de electricidad para separar los átomos de un compuesto molecular. En las reacciones redox, mención especial merecen los llamados radicales o radicales libres que tan mala propaganda tienen, con toda la razón del mundo. Cuando estos traspasan un cierto umbral, son nocivos para nuestro cuerpo y provocan la aparición de numerosas enfermedades. Se nos bombardea continuamente acerca de los daños que producen dichos radicales: el envejecimiento, el cáncer, las enfermedades del Parkinson y Alzheimer, etc. Fumar y, en general, los malos hábitos, aumentan el número de radicales libres en nuestro organismo. Nosotros somos capaces de asimilar un cierto número de radicales libres, es decir, los que se generan de una manera natural (por ejemplo, a partir del metabolismo o neutralizando el ataque de los virus y las bacterias).
Los radicales libres intervienen también en los procesos de señalización de las células y activan mecanismos vitales. Los radicales libres reaccionan químicamente con otras moléculas alterando su estabilidad y funcionalidad dentro del organismo. De sobra conocido es que la forma más efectiva de combatir la presencia de radicales libres es a través de antioxidantes (vitaminas, minerales, etc.) que retardan o previenen la oxidación de otras moléculas. En general, las moléculas tienen todos los electrones en sus estados de energía formando parejas; es decir, según el principio de exclusión de Pauli, en cada nivel de energía de la molécula hay dos electrones con espines antiparalelos. El espín total de la molécula es por tanto cero. No obstante, hay moléculas que tienen algún electrón libre en su capa más externa ya que el resto de los electrones están todos pareados o emparejados y presentan una gran avidez a buscar pareja. De esta forma, estas moléculas son muy activas e inestables participando en un gran número de reacciones químicas, al igual que ocurre con los radicales.
Es muy ilustrativo analizar, de nuevo, la formación de agua a partir de sus elementos ya que nos permite introducir un concepto básico que es la energía de activación de una reacción química. La reacción química es
2 H2 (g) + O2 (g) → 2 H2O (g),
donde el hidrógeno molecular (H2) está formado por dos átomos de hidrógeno unidos por un enlace covalente (H-H) y el oxígeno molecular (O2) cuyos átomos están unidos por un enlace covalente doble (O = O). Esta reacción no tiene lugar mientras los enlaces covalentes no se rompan, de otra forma, estas dos moléculas podrían estar siempre cerca la una de la otra sin que se produjera nunca la reacción. La energía suministrada por una chispa eléctrica desencadenaría automáticamente la reacción pues rompería los enlaces covalentes de los reactivos. El hidrógeno y el oxígeno atómicos son muy reactivos haciendo que la velocidad de formación del agua sea muy rápida. Esa energía suministrada se conoce como energía de activación. Los reactivos poseen, en general, una energía mayor que la de los productos, liberándose entonces una gran cantidad de energía (reacción exotérmica). Este proceso queda recogido gráficamente en la figura 4.
Esta figura debe entenderse como un mapa de energía. En el máximo de energía, los reactivos están formando un compuesto denominado complejo activado o estado de transición que dura un breve lapso. Este tiempo es el que necesitan los átomos de hidrógeno y oxígeno para acomodarse para la formación de los nuevos enlaces que forman la molécula del agua.
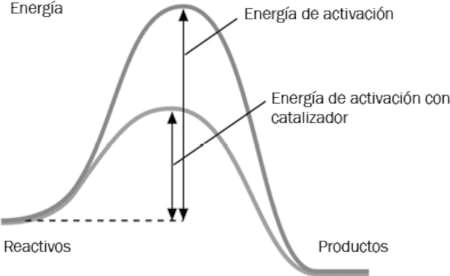
Figura 4. Esquema energético de una reacción química exotérmica. La energía de activación es la energía que se necesita para que tenga lugar la reacción y la diferencia de energía entre reactivos y productos, la energía que se desprende. El máximo de energía corresponde a lo que se conoce como complejo activado o estado de transición. Un catalizador sirve para disminuir la energía de activación.
En general, deberíamos escribir mejor la reacción química como sigue:
A + B → estado de transición → C + D.
Esta teoría se conoce como la teoría del estado de transición. Una imagen que ayuda a comprender esta figura es la siguiente. Imaginemos que donde están los reactivos tenemos una grancantidad de agua que está a una determinada altura y, por tanto, posee una energía potencial. Queremos trasladar la cantidad de agua que hay en la zona de reactivos a la zona de productos, que está a una altura menor. Como en los pantanos, la diferencia de altura puede generarnos energía eléctrica, ya que en la zona de productos tenemos un sistema de turbinas que se mueven al caer el agua. Tenemos un inconveniente, hay una montaña que separa ambas zonas. Podemos consumir energía para elevar el agua en la zona de los reactivos (energía de activación) por encima del pico de la montaña para vencer este obstáculo. Este esfuerzo o trabajo realizado valdrá la pena si conseguimos pasar el agua a la zona de productos y la energía que obtenemos es mayor que la gastada en elevar el agua.
Lo mismo pasa con una reacción química. Esta energía de activación también se puede suministrar en forma de calor, aumentando la temperatura para que suministre una energía como mínimo igual a la de activación. Pero como ya somos expertos en mecánica cuántica, cuando se habla de montañas, barreras u obstáculos, debemos tener también presente el efecto túnel. Hay muchas reacciones químicas que ocurren a bajas temperaturas, no teniendo suficiente energía para superar la montaña; entonces si los reactivos tienen poca masa (como el H, por ejemplo) se abre un túnel en la montaña para que pueda pasar el agua de reactivos a productos. Con otras palabras, el gato, que está a la izquierda en el agua nadando, tiene pereza o no puede sortear la montaña, entonces decide abrir un túnel, como si fuera un topo, pasando a la derecha, feliz y contento.
§. Isómeros, enantiómeros y tautómeros
Imaginemos que tenemos solo unas cuantas fichas de LEGO, ¿cuántas figuras se pueden hacer con ellas? En principio, si hay suficientes fichas, al menos más de una. Pues esto también pasa con las moléculas orgánicas. De acuerdo a la figura 5, una misma fórmula molecular puede conllevar dos estructuras diferentes; por ejemplo, la fórmula química C2H6O puede representar el alcohol etílico y el éter dimetílico, sustancias con propiedades radicalmente diferentes. También podemos imaginar que una rotación simple puede llevarnos a dos estructuras diferentes como, por ejemplo, la molécula 2-buteno. En este caso, las posiciones del H y del grupo CH3 (grupo metilo) se intercambian por una mera rotación respecto a un carbono del enlace covalente doble. En química orgánica, cuando los mismos grupos están arriba o abajo, se les denomina isómero cis (o conformación cis), cuando están intercambiados, isómero trans (o conformación trans). Si dos isómeros presentan diferente actividad óptica, es decir, se comportan de forma diferente cuando incide la luz en ellos, se les llama enantiómeros. Estos isómeros serán especialmente importantes cuando tratemos, más adelante, la quiralidad.
Otros isómeros que juegan un papel esencial en la biología molecular son los tautómeros, donde existe una migración o desplazamiento de un átomo o grupo de átomos a otras posiciones dentro de la molécula, cambiando de nuevo las propiedades químicas.
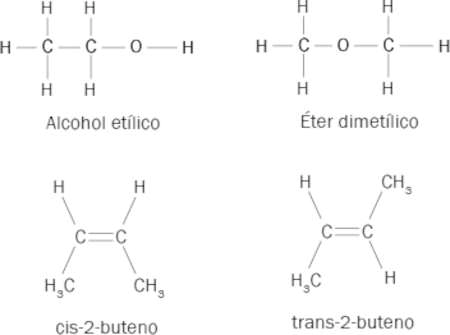
Figura 5. Isómeros con fórmulas químicas C2H6O para el alcohol etílico y éter dimetílico y los isómeros cis y trans de la molécula 2-buteno.
En todos los casos que hemos mencionado, el entorno influye para tener la presencia y el predominio de un isómero respecto al otro (por ejemplo, la temperatura, un medio ácido o básico, etc.). Normalmente, la dinámica de los dos isómeros puede verse como resultado de una reacción química donde uno hace el papel de reactivo y el otro de producto. El entorno químico o físico existente hace que la doble flecha (reversibilidad) de la reacción se decante más hacia un lado que hacia el otro.
§. Las proteínas y enzimas
En 1950 ya se aceptaba que el conocimiento de la estructura de las moléculas proteicas (o proteínas) es tan importante para la biología como la estructura atómica para la física. Como ya hemos dicho, la actividad biológica de las proteínas, las enzimas, las hormonas, las vitaminas, los anticuerpos, los genes, etc., deriva muchas veces de su estructura molecular. La palabra proteína viene del griego que significa «de principal o primer orden» y fue acuñada por el químico holandés G. J. Muldner a sugerencia del químico sueco J. J. Berzellius.
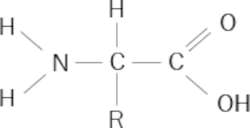
Figura 6. Fórmula química de un aminoácido. El grupo carboxilo (COOH) tiene carácter ácido (es capaz de liberar protones, H+) y el grupo amino (NH2) carácter de base (capaz de atraer protones). R es una cadena lateral o radical formada por un solo átomo como el H o mucho más complicada formada por grupos de átomos; por ejemplo, R podría ser – CH3, —CH2 —CH2 —COOH, —CH2 —CONH2, etc.
La ciencia bioquímica quizás comenzó en 1828 cuando F. Wöhler sintetizó accidentalmente, y por primera vez, un producto elaborado por los organismos vivos como la urea (NH2-CO-NH2) a partir de compuestos inorgánicos (cloruro de amonio o sal de amoníaco, NH4Cl, y cianato de potasio, KOCN), poniendo fin a la teoría imperante de la época debida a Berzellius y denominada teoría vitalista, que afirmaba que la actividad de los seres vivos se debía a una fuerza vital especial. El puente entre la materia inanimada (inorgánica) y la animada (orgánica) había sido establecido de una forma clara y patente o, al menos, así se pensaba en la época.
Las proteínas son macromoléculas (moléculas muy grandes) formadas por cadenas lineales de ciertas unidades químicas llamadas aminoácidos que podrían considerarse como los átomos biológicos. Los 20 aminoácidos que constituyen las proteínas (aminoácidos proteicos) tienen la estructura ilustrada en la figura 6. Algunos de ellos son ya familiares por el interés creciente de las personas sobre la dieta (por ejemplo, ácido glutámico, cisteína, lisina, ácido aspártico, alanina, glicina, triptófano, etc.). Sus extremos tienen propiedades químicas distintas, uno de ellos tiene carácter de base y el otro de ácido, permitiendo la unión de ellos, gracias a los protones (H+), por sus extremos para formar largas cadenas moleculares. En esas uniones se elimina, como ya hemos visto anteriormente, agua y se forma el llamado enlace peptídico (figura 12). Cuando se unen dos aminoácidos tenemos un dipéptido y cuando se unen muchos, un polipéptido o proteína. El número mínimo de aminoácidos necesarios para formar una proteína se establece, según algunos autores, a partir de 50 o 100. Cada aminoácido puede verse como la perla de un collar, el eslabón de una cadena o la cuenta de un rosario.
En 1953, el bioquímico inglés F. Sanger, doblemente laureado con el Nobel de Química como M. Curie, L. Pauling y J. Bardeen, y sus colaboradores determinaron por primera vez la secuencia de los 51 aminoácidos que forman la insulina, generada por el páncreas y primordial para controlar el paso de la glucosa desde la sangre a las células de los tejidos. Como es sabido, su escasez causa la diabetes mellitus. Esta proteína fue sintetizada in vitro en 1966. Se ha establecido una analogía utilizada en la actualidad entre la secuencia de aminoácidos de una proteína y la secuencia de letras y espacios que forman una frase. Al igual que el orden de las letras en una palabra y en una frase determina su sentido o significado, el orden de los aminoácidos determina su actividad biológica. Si ligeras modificaciones en una frase pueden mantener su significado fundamental, lo mismo ocurre con los aminoácidos en los diferentes organismos vivos, sin deteriorar su actividad biológica. Al final, la estructura tridimensional de las proteínas, derivada de la secuencia de sus aminoácidos, marcará su actividad biológica.
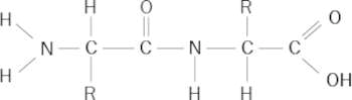
Figura 7. Enlace peptídico formado por la unión de dos aminoácidos.
Esta analogía es de aplicación limitada pues, en sentido estricto, la actividad biológica está determinada por más factores tales como el entorno, las interacciones con otras moléculas, etc. No obstante, unhecho fundamental es que las proteínas difieren marcadamente de un organismo a otro. Como sabemos, este es un problema crítico que se intenta superar en la investigación de trasplantes. Las macromoléculas del órgano del donante son rechazadas por el cuerpo receptor mediante los anticuerpos al reconocerlas como cuerpos extraños, ya que las secuencias de aminoácidos son diferentes. Pero no es menos cierto que en la actualidad se pueden sintetizar proteínas e insertar cualquier aminoácido en la posición de la cadena que se quiera. El diseño de nuevos fármacos avanza en esa dirección.
La estructura de las proteínas puede considerarse dividida en cuatro niveles. La estructura primaria está representada, como he mencionado anteriormente, por la secuencia de los aminoácidos unidos mediante el cemento resistente de los enlaces covalentes (principalmente, los enlaces peptídicos). Esta cadena de aminoácidos se encuentra frecuentemente enrollada en una o varias configuraciones no necesariamente helicoidales mediante enlaces más débiles como el enlace de hidrógeno y se habla de la estructura secundaria. A su vez estas cadenas pueden enrollarse y plegarse para formar figuras geométricas tridimensionales más complicadas mediante enlaces aún más débiles como el de Van der Waals, dando lugar a la estructura terciaria. La actividad biológica de las proteínas se debe a esta estructura terciaria frágil y flexible, ya que está construida mediante enlaces muy débiles. Esta actividad biológica deja de funcionar cuando la proteína, por ejemplo, se desnaturaliza, es decir, cuando se expone a condiciones físicas o químicas adversas.
No siempre este proceso es reversible. En general, la pérdida de la actividad biológica puede deberse a cambios muy sutiles o a perturbaciones que afecten a los sitios activos de las proteínas o a sus interacciones con otras proteínas, o con genes u otras moléculas. La actividad biológica es muy compleja y puede verse afectaba por sutiles y pequeñas perturbaciones. Las proteínas dúctiles o desordenadas juegan un papel esencial. La predicción de la estructura terciaria a partir de la primaria no es obvia y, muchas veces, se tiene un catálogo de correspondencia entre ambos niveles construido a partir de la propia experiencia.
El tránsito de la estructura primaria a la terciaria se conoce como plegamiento de las proteínas. El fallo en el proceso de plegamiento puede llevar muchas veces a la aparición de enfermedades graves como el cáncer, Alzheimer o Parkinson. Se pensaba que este proceso estaba regido por las leyes de la física clásica. Pollak sugirió recientemente que el efecto túnel puede también estar detrás de esta dinámica y observó que el tiempo de plegamiento, por este efecto, disminuye a medida que la temperatura se reduce. La agrupación de las proteínas para formar estructuras más grandes y complejas constituye la estructura cuaternaria, dando lugar a nuevas actividades biológicas importantes en la vida a nivel celular y, por tanto, importante para la arquitectura de la vida.
Existe un largo camino a recorrer en la dirección de acumulación de conocimientos sobre la secuencia de aminoácidos y estructuras tridimensionales (como un coleccionista de sellos) y la comprensión de la correspondiente actividad biológica. Dos tipos de proteínas que merecen destacarse son las fibrilares, que son utilizadas principalmente por el organismo como proteínas estructurales y constituyen el material del que están formados los tendones y ligamentos, las plumas, la lana, el pelo, las garras, las uñas, etc., y las globulares, más complejas, que actúan como enzimas, trasportadoras de oxígeno, anticuerpos, estructuras propulsivas (como, por ejemplo, los músculos, flagelos y cilios). En la estructura cuaternaria entran en juego las proteínas globulares y, en menor medida, las fibrilares. Las propiedades más reseñables de las proteínas son la flexibilidad y la plasticidad (susceptibles de ser moldeadas para cambiar de forma).
En los años sesenta del siglo pasado se creía que las proteínas obedecían a estructuras tridimensionales siguiendo un plan definido. La difracción por rayos X y el microscopio electrónico son dos técnicas experimentales ampliamente utilizadas para el análisis de la estructura tridimensional de las proteínas. Las primeras analizadas por rayos X fueron la pepsina, insulina, mioglobina y hemoglobina. Hoy en día, hay muchos más métodos experimentales para su caracterización. La era de la proteónica acaba, como quien dice, de empezar.
En los procesos vitales, las enzimas, que son proteínas globulares, juegan un papel primordial en la reactividad química aumentando la velocidad de reacción para facilitarla, como hacen los catalizadores. Estos proporcionan un mecanismo o proceso de reacción alternativo, disminuyendo la energía de activación junto con la formación de un estado de transición diferente (figura 4). En otras palabras, «engrasa» el mecanismo de la reacción química. La enzima se une a los reactivos, forma el estado de transición para después dar lugar a los productos, liberándose de nuevo la enzima de acuerdo a la reacción
A + B + enzima → estado de transición → C + D + enzima.
Al ser una proteína, solo una pequeña región de su estructura terciaria es la que participa en la reacción. Esta zona activa se «fija» a los reactivos mediante enlaces débiles como los de hidrógeno y de Van der Waals, pues si fueran covalentes, que son mucho más fuertes, su liberación posterior retrasaría enormemente la reacción. Las enzimas son selectivas en el sentido de que cada reacción química vital requiere una enzima particular. Las enzimas requieren muchas veces la presencia de iones metálicos como K+ (ion potasio), Ca2+ (ion calcio) y Mg2+ (ion magnesio) u otras moléculas orgánicas llamadas coenzimas para realizar su actividad. Como comprenderá el lector, esto es un mundo apasionante pero complejo por la variedad y la riqueza de los procesos químicos esenciales para la vida.
A las enzimas se les conoce también como máquinas (mejor dicho, nanomáquinas) moleculares o motores de la vida ya que aceleran toda clase de reacciones bioquímicas de un organismo vivo, el proceso del metabolismo. Si no existiera esta actividad enzimática, los procesos que tienen lugar en las células podrían demorarse hasta miles de años en vez de segundos o incluso menos. No se comprende del todo bien, a día de hoy, la actividad enzimática. De hecho, aún no se ha podido sintetizar una enzima partiendo de cero y que pueda llegar al aumento notable de las velocidades de reacción alcanzadas por las enzimas naturales. Lo que sí parece bastante probable es que ayuden o participen para que el efecto túnel de los electrones y los protones tenga lugar.
La importancia de las enzimas es sin lugar a dudas remarcable. La función más importante es conseguir que la cantidad de reacciones químicas (que son millones) en los organismos vivos ocurran simultáneamente y a cada instante, en tiempos cortos compatibles con la vida de cada uno de ellos. Se las conoce también como biocatalizadores o catalizadores biológicos y son específicas para una o pocas reacciones químicas, pudiendo regular su actividad en función del medio que les rodea. A lo largo de la evolución, las enzimas pasaron de ser generalistas (estaban involucradas en muchos procesos químicos) a ser mucho más específicas. Otra propiedad sorprendente de las enzimas es que son capaces de regular su actividad en función de su entorno (como si fueran camaleónicas). Aparte de esta actividad tan básica, sus potencialidades son también numerosas. Por ejemplo, permiten diagnosticar enfermedades y están presentes en la industria química, farmacéutica y alimentaria.
© 2026 JAVIER DE LUCAS