QUIMICA FARMACEUTICA

Anteriormente, las farmacias se enfocaban únicamente a desarrollar
formas para la administración y aislamiento del principio activo, como son las
tinturas, la maceración, las pomadas y los jarabes, entre otras; conocimiento
adquirido por años de estudio de las antiguas culturas. Para 1920-1930 las
drogas sintéticas hacen su aparición, principalmente por la creación de las sulfas.
La mayoría de las nuevas drogas incluye productos de la química
orgánica sintética, aunque aún se encuentran principios activos de origen
natural, sobre todo la mayoría de los antibióticos; sin embargo, incluso en
este último grupo, la química se volvió importante para su producción en
grandes cantidades y la búsqueda de la pureza adecuada, con el objetivo de tener
compuestos más potentes o con mayor eficacia que los naturales.
La química farmacéutica es una rama de la farmacología cuyo
objetivo es el estudio de fármacos e involucra los aspectos en la producción
del mismo, desde su síntesis, aislamiento y sus acciones terapéuticas para una
patología específica, intentando comprenderlos a nivel molecular por las
características químicas del fármaco. Actualmente se sabe que la capacidad de
una droga para desempeñar la acción deseada a nivel de órgano diana depende de
tres características de la molécula: el tamaño, la forma y el grado de
ionización; si la molécula llega a modificarse en alguna de estas tres
características, entonces la acción del fármaco cambiaría con un aumento en la
actividad o viceversa.
Para comprender mejor las variaciones que puede tener la acción de
una droga según las modificaciones en su molécula y como ésta puede mejorar o
disminuir su acción terapéutica se emplea el enfoque analógico
Enfoque
analógico
Esta es la forma más utilizada de obtener drogas que se utilizarán
en la terapéutica de patologías específicas. Como su nombre lo indica, consiste
en la creación de análogos de una molécula farmacológica previa, conocida por
tener una eficacia para tratar determinada enfermedad. Sirve como “molécula
guía” para buscar una nueva actividad biológica, mayor potencia en menor dosis,
disminuir la toxicidad del fármaco, mayor selectividad y mayor o menor duración
de la actividad de la droga.
Tamaño
Según el tamaño de las moléculas podemos tener:
Homólogos
Son análogos en los que cambia la estructura de la molécula guía
por el incremento o disminución en la formula molecular, como es el incremento
o reducción en la cadena de carbonos. Se utiliza para conocer la relación que
existe en la actividad terapéutica de un fármaco con la longitud de la molécula
o en otras palabras, su cantidad de grupos metilos (CH3). Por lo
regular se considera que conforme las cadenas alquílicas aumentan de tamaño,
mayor será su acción hasta llegar a un punto inmejorable para la terapéutica,
del cual si se continúa incrementando el número de cadenas vuelve a disminuir
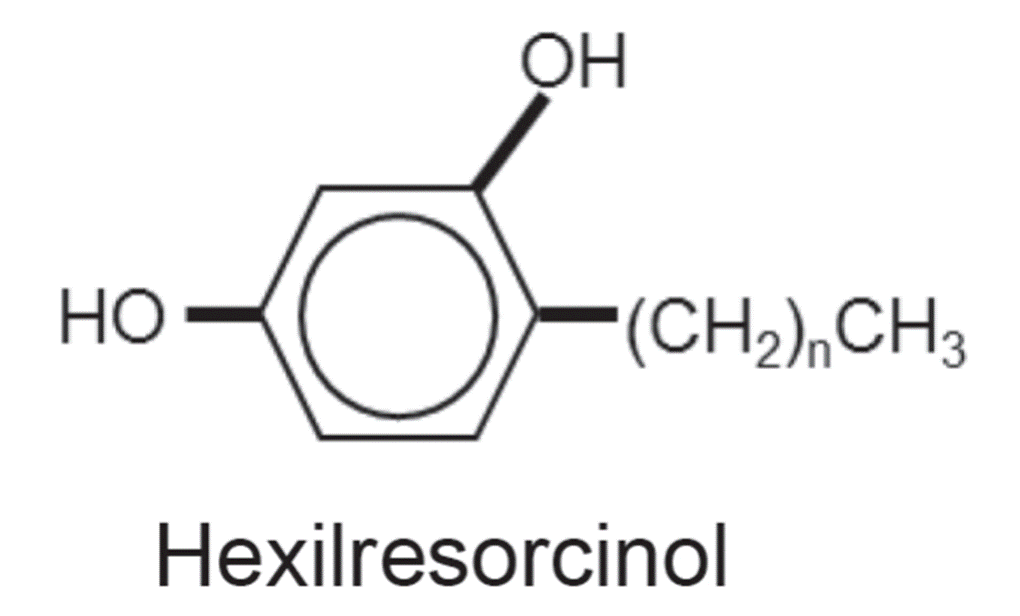
la eficacia. Por ejemplo, la actividad de los compuestos fenólicos frente a B. typhosus, medida por el coeficiente de fenol logra su
actividad optima cuando es hexilresorcinol, que
cuenta con una cadena de 6 átomos de carbono en su cadena lateral. Si
disminuyéramos o aumentáramos la cadena alquila la efectividad de la molécula
frente a B. typhosus disminuiría.
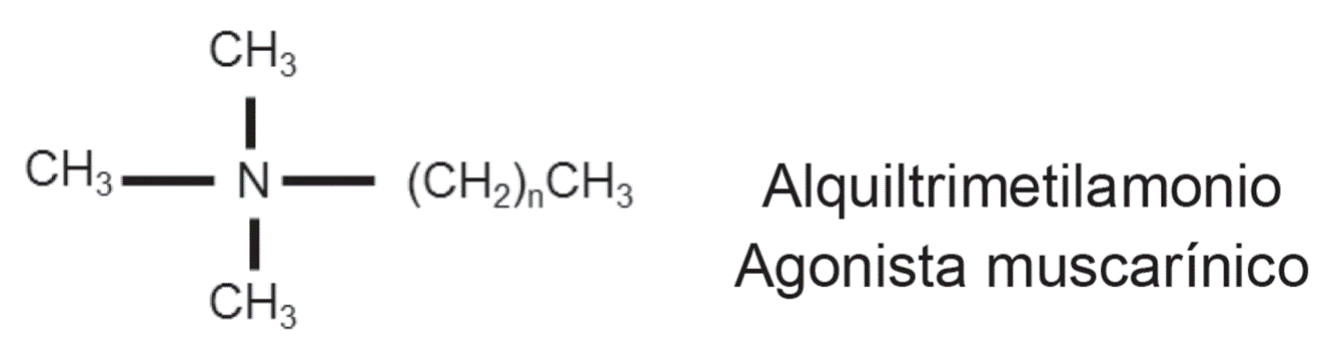
Hay ocasiones en que el cambio en el número de grupos metilos
puede modificar la actividad de la molécula y no su potencia de acción, como en
el caso de los análogos de alquiltrimetilamonio cuyo
compuesto tiene seis carbonos. Esta molécula funcionaría como agonista muscarínico semejando la acción de la acetilcolina en el
cuerpo humano; si al análogo se le aumenta a 7 u 8 carbonos, la molécula sería
un agonista parcial; si contara con más de 9 carbonos, su acción buscaría
contrarrestar la actividad de la acetilcolina, es decir, se convierte en
antagonista muscarínico.
Fragmentación
molecular
Esta es otra manera de observar la importancia que tiene la
naturaleza química de una droga. Una molécula puede ser simplificada en
estructura pero mantener la misma actividad en el organismo o continuar con la
misma actividad biológica, pero llevándola acabo de manera distinta. Un ejemplo
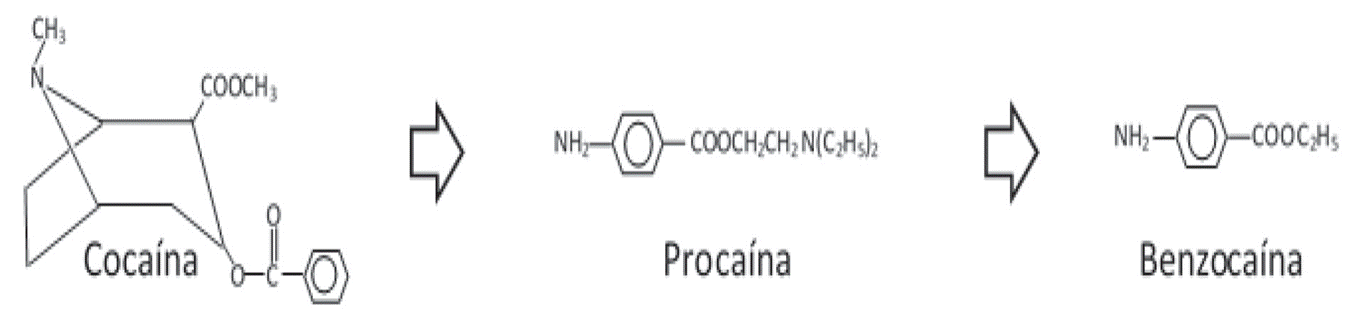
de la simplificación que se le puede hacer a una droga es la cocaína, que tiene
actividad de anestésico local. Si se disocia de la molécula guía el grupo carbometoxi y el anillo tropano,
la actividad anestésica se mantiene. La síntesis de procaína,
molécula con segmento amínico hidrófilo fijado a una cadena intermedia que se
une a la función éster lipófila, es la parte necesaria para mantener la
actividad de anestésico local, y si a su vez a la procaína
se le elimina la sección amina, nos da benzocaína que sigue teniendo la misma
actividad como anestésico local pero con diferente mecanismo de acción.
Esta fragmentación molecular ayuda para la comprensión de la
relación estructura-actividad que existe y para la producción de fármacos
cuando la base del principio activo proviene de un origen natural que puede ser
de difícil acceso para su producción industrial, además ayuda a aumentar la
pureza de la droga disminuyendo los efectos indeseables causados en la molécula
guía.
Forma
Estereoquímica
Los isómeros son aquellos compuestos que poseen diferentes
funciones físicas o químicas pero que tienen una misma fórmula molecular. Al
momento de ver el mecanismo de acción de una droga es importante tener en
cuenta la estereoquímica de la molécula, considerando que al cambiar alguna de
los grupos funcionales de la molécula, la actividad droga-receptor o enzima
puede variar. Hay distintas formas de isomería: la posicional, geométrica y
óptica, entre otras.
Posicional
En este tipo de isómeros, como su nombre lo indica, la molécula
cuenta con la misma fórmula pero los grupos funcionales están en un orden
distinto, lo que puede variar su actividad terapéutica cuando hablamos de una
droga. Un ejemplo son un par de barbitúricos, el pentobarbital
y el amobarbital.
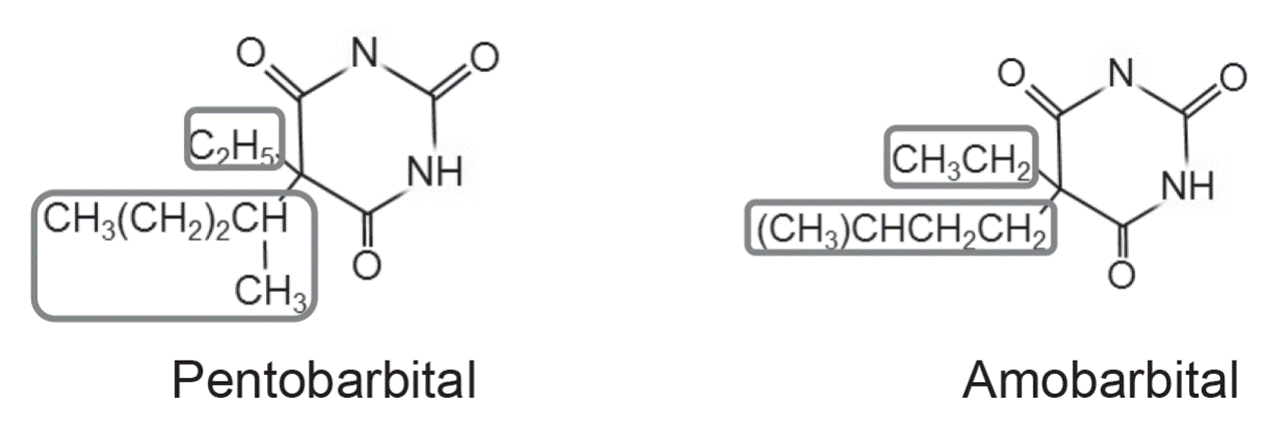
Ambos difieren en su conformación molecular a nivel de 5 carbonos
ubicados en su cadena lateral que se fija a su anillo barbitúrico, lo que
modifica la duración de su acción farmacológica: mientras el pentobarbital tiene una acción corta el amobarbital
es de acción intermedia.
Geométricos
En estos isómeros los grupos funcionales tienen sus enlaces al
mismo carbono pero poseen una localización diferente en la molécula. En estos
compuestos sus propiedades a nivel fisiológico pueden cambiar enormemente,
pueden ir desde sólo disminuir en su potencia o en uno ser biológicamente
activo y en el otro no tener actividad fisiológica alguna.
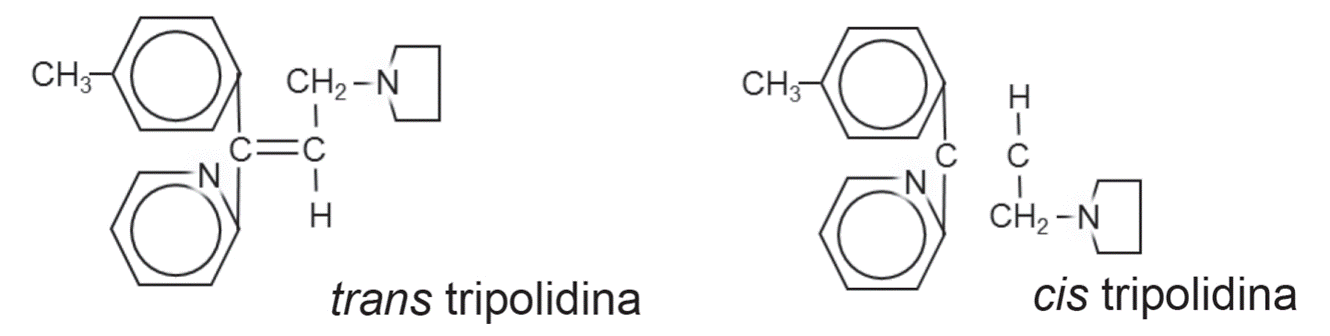
El isómero trans de tripolidina
es 1.000 veces más potente que el isómero cis como
antagonista histamínico
Ópticos
Los isómeros ópticos son moléculas que son imágenes especulares; a
pesar de esta variación mínima, sus propiedades físicas son idénticas pero
difieren en la rotación de la luz polarizada, aunque en ocasiones pueden variar
la intensidad de sus acciones. Ejemplos de estas moléculas son el isómero R (-)
adrenalina que es más potente en receptores alfa adrenérgicos y beta
adrenérgicos que el isómero S (+) adrenalina.
Es importante siempre tener en cuenta que incluso las variaciones
en el tamaño o las más mínimas variaciones en la forma de una molécula, en la
manera en que se distribuyen sus grupos funcionales, tendrán implicaciones en
cómo desarrolle su acción un fármaco, que pueden ser en mayor o menor potencia.
Grado de
ionización
A un amplio número de las drogas usadas en la terapéutica podemos
clasificarlas como ácidos débiles o bases débiles, que se pueden encontrar en
una solución en su forma ionizada (A- + H+) o no ionizada (HA). Las moléculas
no ionizadas tienden a ser de carácter liposoluble por lo que pueden atravesar
membranas plasmáticas, mientras las formas ionizadas tienen nula o poca liposolubilidad por lo que su paso a través de las
membranas depende principalmente de la permeabilidad de la membrana; esto tiene
una relación con la carga eléctrica de la membrana que tiende a ser negativa,
entonces la capacidad de estos fármacos para realizar su acción dependerá de la
cantidad de fármaco que permanezca en forma no ionizada o ionizada.
El pKa es el pH en el cual la mitad del
fármaco se encuentra en su forma no ionizada y la mitad en forma ionizada. En
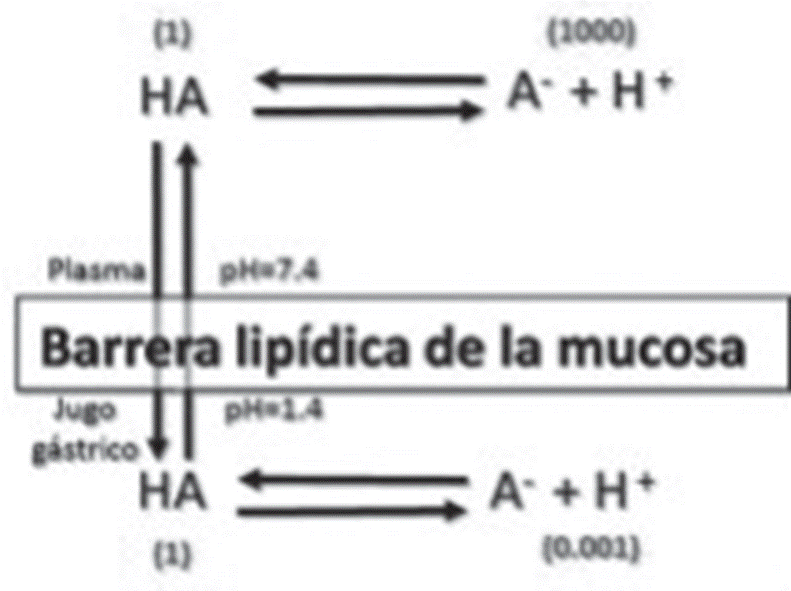
la siguiente imagen se ilustra el modo de distribución de un fármaco que es
ácido débil y tiene un pKa de 4.4, entre el jugo
gástrico con un pH de 1.4 y la sangre con pH de 7.4, considerando la presencia
de la mucosa gástrica (la cual es permeable a la forma no ionizada), el
transporte del fármaco de un compartimiento a otro variara por la diferencia de
pH.
Para conocer la relación entre la forma ionizada y la no ionizada
según el pH del medio se utiliza la fórmula de Henderson-Hassel-Bach:
pKa = pH + log
(forma ionizada) / (forma no ionizada)
En el ejemplo del fármaco ácido débil la relación de forma no
ionizada/ionizada en el plasma es 1:1000 y en el jugo gástrico es 1:0.001.
Vemos que la tendencia del fármaco de encontrarse en una forma predominante no
ionizada en el jugo gástrico y en una forma ionizada en el plasma que disminuye
su paso a través de la mucosa hace que el fármaco se encuentre en una cantidad
mayor en un pH que tiende a la alcalinidad. Si cambiáramos a uno que es una
base débil, la mayor distribución del fármaco sería en el medio que tiende a la
acidez. Entonces, un fármaco ácido predomina en el medio que tiende más a la
alcalinidad y un fármaco básico predomina en el medio más ácido.
La importancia de tener en cuenta esto es que el grado de
ionización de la molécula tendrá implicaciones en la distribución de los
distintos compartimientos en el cuerpo humano y, por lo tanto, se infiere que
tendrá implicaciones principalmente en la absorción, concentración y
eliminación de un fármaco. Ejemplo de esto es la eliminación de un fármaco a
través de la vía renal, el pH urinario tiende a variar desde 4.5 a 8. En los
túbulos renales los fármacos no ionizados, es decir liposolubles, pueden
reabsorberse por difusión pasiva y disminuir o retardar la eliminación del
fármaco, entonces la eliminación de un fármaco ácido débil (ácido
acetilsalicílico) puede aumentarse si se modifica el pH urinario para hacerlo
ir hacia la alcalinidad.
NOMENCLATURAS
El conocimiento y manejo correcto de la nomenclatura de los
diversos fármacos existentes es un asunto de gran relevancia para búsqueda de
información y referencias bibliográficas, y representa el consenso que debe
existir para un manejo de medicamentos coordinado y que evite confusiones.
Nomenclatura experimental
El descubrimiento de un nuevo principio activo o la creación de un
nuevo fármaco involucra la denominación de una
sustancia nueva, que debe pasar por ciertas etapas hasta la designación de un
nombre comercial. A partir de que es descubierto, el fármaco recibirá un nombre
provisional que lo identificará desde la investigación y durante las diferentes
fases de la experimentación. A esto se le denominará código de laboratorio.
Este código estará conformado por una combinación de letras y
números relacionados con la empresa o laboratorio que esté desarrollando el
fármaco respectivo. No tiene ningún carácter oficial y no está regulado por
ninguna institución más que la que lo crea, pero es gran utilidad para su
referencia bibliográfica en la publicación de diversos resultados donde se
muestren las pruebas realizadas con ese fármaco mientras se estudia. Un
ejemplo de una su estructura podría ser la siguiente: ABT-450.
Nomenclatura química
Denominación otorgada por la Unión Internacional de Química Pura y
Aplicada (IUPAC), por sus siglas en inglés) o la Unión Internacional de
Bioquímica y Biología Molecular (IUBMB), por sus siglas en inglés), que hace
referencia a la composición molecular del principio activo en sí. Este nombre
permite la identificación del compuesto de manera global, entre los químicos y
demás profesionales informados en el tema, a manera de que se genere un
consenso en la información y se eviten confusiones para su referencia y
descripción. Además también permite tener un reconocimiento previo de las
cualidades de la sustancia, en base a sus características químicas. Sin
embargo, debido a su complejidad, a que no es fácil de recordar y a que es
incomprensible para aquellos que no estén relacionados con el tema, no es de
las nomenclaturas más usadas. Pero eso no le resta importancia ni la necesidad
de ser implementada. Un ejemplo de esto sería la nomenclatura del paracetamol
según la IUPAC: N-(4-hidroxifenil) etanamida.
Nomenclatura de genéricos
Para facilitar una identificación más globalizada y sobre todo
para la mayor comprensión y uso de fármacos, la Organización Mundial de la
Salud (OMS) determinó una resolución para la creación de un sistema de
“Denominación Común Internacional” (DCI) de los principios activos en el año de
1950. Estos también son conocidos como nombres genéricos o por su equivalente
en el idioma inglés, International Non-propietary Names (INN).
Esta designación de nombres se hace a partir de un comité
especializado de la OMS, que publicó en 1953 la primera lista de es Manual de
conocimientos básicos de farmacología tas denominaciones. Se genera un acuerdo
con las organizaciones reguladoras en materia de salud de cada país y así se
genera un acuerdo global para el nombramiento de los diversos principios
activos. Para esto, se hace uso de reglas de prefijos y sufijos que sirven para
identificar a un gran grupo farmacológico específico con características
similares. Con esto se busca que se eliminen la mayor cantidad de confusiones
que puedan surgir con la mención de un nuevo fármaco, y que además facilite el
uso de los medicamento de manera universal. En caso de no tener una denominación
común internacional, se utiliza la denominación común usual o la científica del
compuesto, acompañada del nombre o marca del titular o el laboratorio
fabricante.
Ejemplo de esto sería el siguiente: la cefalexina
utiliza el prefijo “cef”, que indica que es un
antibiótico derivado del ácido cefalosporánico, al
igual que la cefradrina. Pero también existe el uso
de sufijos como “bactam”, utilizado para los fármacos
inhibidores de las β-lactamasas como el sulbactam o el tazobactam.
Nomenclatura comercial
Es el nombre dado por la empresa farmacéutica encargada de su
distribución y venta, una vez que logra su patente y pasa por todas las pruebas
necesarias para su aprobación de uso clínico. Durante esta etapa, hablando
sobre todo del desarrollo de nuevos fármacos, la fórmula puede no ser revelada
completamente para protegerla del plagio. Esta patente debe ser respetada por
aquellas naciones que integren el convenio respectivo, y generalmente tiene una
duración máxima de 20 años. Durante este tiempo, ningún otro laboratorio podrá
reproducir un fármaco a partir de ese compuesto, lo que permite la exclusividad
del aprovechamiento económico para el laboratorio que la
desarrollo.
Una vez terminado el tiempo de la patente, aquellas empresas
farmacéuticas que lo deseen y tengan la capacidad para reproducirlo, podrán
elaborar el fármaco, distribuirlo y venderlo de manera nacional o
internacional, promoviendo así la competencia económica. El dueño original de
la fórmula puede decidir si vende su principio activo a otras empresas y
permite el uso de su derecho para producirlo y venderlo. Generalmente este
suele ser de los nombres más recordados por los pacientes, por lo que es
recomendable que los médicos estén familiarizados con él pero siempre
recordando la denominación común del medicamento y, sobre todo, los mecanismos
de acción que tiene sobre el organismo.
Un ejemplo de esto lo encontramos en el paracetamol, que es más
conocido por su nombre comercial Tempra®.
Importancia
y diferenciación de genéricos intercambiables
Los medicamentos genéricos son aquellos que tienen una
composición, tanto cualitativa como cuantitativa, similar a la del fármaco que
se busca reproducir. Tiene la misma presentación, y su bioequivalencia
con el medicamento de referencia es demostrada por análisis y pruebas a cargo
de laboratorios certificados que determinan si tiene un comportamiento similar
en el organismo.
Estos medicamentos tienen un menor precio que los de patente
porque su inversión en desarrollo y comercialización es mucho menor, lo que
facilita su acceso a una mayor cantidad de consumidores. Además, el laboratorio
no tendrá que invertir tanto en mercadotecnia y evitará el retraso que implica
la aprobación de organismos internacionales para su uso clínico. Otro detalle
destacable es que su nombre coincide con el del principio activo y esto hace
más fácil su identificación. Sin embargo, se asocia a una mala adherencia al
tratamiento porque en ocasiones la presentación pude variar en cuanto a colores
o las características físicas de la píldora o pastilla, y genera confusiones en
los pacientes que ya habían consumido el medicamento de patente previamente,
sobre todo en aquellos polimedicados o que son
adultos mayores.
Bioequivalencia de fármacos
similares
Se habla de bioequivalencia cuando dos
productos tienen una biodisponibilidad similar, determinada por pruebas
experimentales apropiadas y semejantes. La biodisponibilidad es la rapidez con
que se obtiene el mecanismo de acción en relación con la cantidad de fármaco
activo que se absorbe y llega a la célula o tejido diana. Para que un
medicamento genérico cumpla con el acuerdo internacional que regula su
producción, debe tener 20% de tolerancia en biodisponibilidad, aunque varía
según algunos autores y también dependiendo de las condiciones que establezca
cada nación.
© 2025 JAVIER
DE LUCAS