VIRUS POR UN TUBO

Un resfriado nada común
Hace 3.500 años, un erudito egipcio se sentó a escribir el tratado médico más antiguo del que se tiene constancia. Entre las enfermedades que describió en el conocido como papiro Ebers figuraba algo llamado resh. Pese a un nombre tan extraño, sus síntomas —tos y fluido mucoso por la nariz— nos resultan familiares de inmediato. El resh es el resfriado común. Algunos virus son nuevos para la humanidad. Otros resultan oscuros y exóticos. Por el contrario, el rinovirus humano —la causa principal del resfriado común y de los ataques de asma — es un camarada tan viejo como cosmopolita. Se estima que a lo largo de su vida, cada persona permanecerá un año en cama por culpa de los resfriados. En otras palabras, el rinovirus es uno de los virus más exitosos.
Hipócrates, el médico de la antigua Grecia, creía que los resfriados eran resultado de un desequilibrio en el estado de ánimo. Dos mil años después, a principios del siglo XX, nuestros conocimientos no habían avanzado mucho. El médico Leonard Hill concluyó que los resfriados eran producto de los paseos matutinos, al pasar de aires templados a fríos. En 1914, un microbiólogo alemán llamado Walther Kruse dio con la primera pista sólida sobre el origen del resfriado, después de que un ayudante que lo padecía se sonara la nariz. Kruse mezcló la mucosidad de su ayudante con una solución salina, pasó el resultado por un filtro y depositó unas pocas gotas del fluido obtenido en doce de sus colegas. Cuatro de ellos acabaron resfriados. Más tarde Kruse repitió el experimento con treinta y seis estudiantes. Quince de ellos enfermaron. Kruse comparó los resultados arrojados por estos con los de treinta y cinco individuos que no habían recibido las gotas. Solo uno de estos últimos contrajo un resfriado. Los experimentos de Kruse dejaron claro que un pequeño patógeno era el responsable de la enfermedad.
Al principio, muchos expertos pensaron que se trataba de algún tipo de bacteria. Sin embargo, el médico estadounidense Alphonse Dochez lo descartó en 1927. Se dedicó a filtrar la mucosidad de individuos resfriados empleando filtros muy finos, a imagen de lo que, tres décadas antes, había llevado a cabo Beijerinck con la savia de la planta del tabaco. Aunque se hubiera extraído la bacteria, el fluido seguía consiguiendo que la gente enfermara. Solo un virus habría sido capaz de colarse entre los filtros de Dochez.
Fueron necesarias otras tres décadas para que los científicos descubrieran qué virus en concreto se había colado. El más común recibe el nombre de rinovirus humano (rino significa «nariz»). Los rinovirus son de una sencillez pasmosa, con solo diez genes por unidad. (Los seres humanos cuentan con unos veinte mil genes).
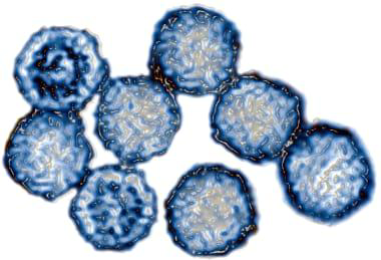
El rinovirus, causa más común de los resfriados
Pese a que la información genética de los rinovirus es comparable a un haiku, les basta para invadir nuestros cuerpos, jugársela a nuestro sistema inmunitario y producir nuevos virus capaces de escapar para ir en busca de nuevos huéspedes. Los rinovirus se propagan a través del goteo de la nariz. La gente resfriada se suena la nariz, los virus van a parar a las manos y luego se diseminan por los pomos de las puertas y el resto de las superficies con las que entran en contacto. Los virus saltan a la piel de aquellos que tocan estas superficies y luego se cuelan en el interior de sus cuerpos, por lo general a través de la nariz. Los rinovirus pueden invadir las células que se despliegan en el interior de la nariz, la garganta y los pulmones. Fuerzan a las células a abrir una trampilla por la que se escurren. Durante las horas siguientes, el rinovirus empleará a sus células huésped para copiar su material genético y las cáscaras de las proteínas que lo sostendrán. Acto seguido la célula huésped se resquebraja y el nuevo virus escapa.
El rinovirus infecta un número relativamente pequeño de células, por lo que causa un daño limitado. ¿Cómo se explica entonces que provoque experiencias tan desagradables? La culpa recae exclusivamente en nosotros. Las células infectadas liberan moléculas señalizadoras, llamadas citocinas, que atraen a células inmunitarias próximas. Son estas células inmunitarias las que nos hacen sentir fatal. Provocan una inflamación que genera una sensación áspera en la garganta y desemboca en la aparición de abundante mucosidad alrededor del foco de la infección. Para recuperarnos del resfriado no solo debemos esperar a que el sistema inmunitario acabe con el virus, sino a que el sistema inmunitario recupere la calma.
El autor egipcio del papiro Ebers escribió que la cura del resh consistía en untarse una mezcla de miel, hierba e incienso alrededor de la nariz. Quince siglos después, el erudito romano Plinio el Viejo recomendaba frotarse un ratón por la nariz. En la Inglaterra del siglo XVII, las curas incluían una combinación de pólvora y huevos, y de estiércol de vaca frito y sebo. Leonard Hill, el médico convencido de que la causa del resfriado yacía en un cambio de temperatura, predicaba que los niños empezaran el día con una ducha fría. A día de hoy seguimos sin un remedio para el resfriado común. El mejor tratamiento con el que hemos dado es el zinc, capaz de bloquear el crecimiento del rinovirus. Aquellos que comienzan a ingerirlo un día después de haber contraído el resfriado pueden reducir la enfermedad en un día o más. Con frecuencia los padres dan jarabe para la tos a sus hijos con el fin de combatir el resfriado, pero los estudios han demostrado que no contribuye a una mejora rápida. De hecho, el jarabe para la tos también acarrea una amplia, si bien rara, variedad de efectos secundarios, tales como convulsiones, aceleración del ritmo cardíaco e incluso la muerte. La Administración de Alimentos y Medicamentos de Estados Unidos advierte de que los menores de dos años —las principales víctimas del resfriado— no deberían tomar jarabe para la tos.
Con excesiva asiduidad los médicos recetan antibióticos a sus pacientes con resfriado. Hablamos de un tratamiento inútil, por cuanto los antibióticos actúan exclusivamente sobre las bacterias y tienen un efecto nulo sobre los virus. Los médicos a veces los recetan porque no saben si el paciente está resfriado o padece una infección bacteriana. En ocasiones quizá respondan a la presión de los padres para que hagan algo. Los antibióticos no solo son inoperantes contra el resfriado. Además suponen un peligro para todos, ya que fomentan la evolución de bacterias de resistencia creciente a los medicamentos, tanto dentro de nuestros cuerpos como en el ambiente. Tratando de forma errónea a sus pacientes, lo que de verdad consiguen los médicos es aumentar el riesgo de que todos padezcamos otras enfermedades.
Uno de los motivos que quizá expliquen las dificultades que encierra el tratamiento del resfriado es que hemos subestimado al rinovirus. Se presenta en muy variadas formas, y solo ahora los científicos empiezan a tomar conciencia de su diversidad genética. A finales del siglo XX, los científicos habían identificado docenas de cepas, pertenecientes a dos grandes familias conocidas como HRV-A y HRV-B. En 2006, Ian Lipkin y Thomas Briese, de la Universidad de Columbia, investigaron la causa de síntomas parecidos a los de la gripe en neoyorquinos que no eran portadores del virus de la gripe y descubrieron que un tercio era portador de una cepa de rinovirus humano que no guardaba una relación estrecha con el HRV-A ni con el HRV-B. Lipkin y Briese la llamaron HRV-C. Desde entonces los investigadores han dado con ejemplos de HRV-C por todo el mundo. Las variaciones en los genes del HRV-C se han revelado escasas de unas regiones a otras. Semejante uniformidad sugiere que esta familia emergió hace unos pocos siglos y se extendió rápidamente por el planeta.
Cuanto más aumenta el número de cepas de rinovirus descubiertas por los científicos, más fácil resulta descifrar su evolución. Todos los rinovirus humanos comparten un núcleo de genes que han permanecido inalterables a lo largo de muchos siglos. En paralelo, unos pocos componentes del genoma del rinovirus están evolucionando a gran velocidad. Estos componentes parecen ayudar al virus a evitar que sea eliminado por nuestro sistema inmunitario. Cuando nuestros cuerpos fabrican anticuerpos susceptibles de detener a una cepa del rinovirus humano, otras cepas siguen siendo capaces de infectarnos porque nuestros anticuerpos no encajan en las superficies de sus proteínas. Esta hipótesis queda respaldada por el hecho de que cada año las personas suelen acabar infectadas por diversas cepas de rinovirus humano.
La diversidad de rinovirus humanos provoca que sean un objetivo muy difícil de neutralizar. Un medicamento o una vacuna que ataquen a una proteína en la superficie de una cepa pueden demostrarse inservibles contra otras que posean una versión de esa proteína con una estructura diferente. Si otra cepa de rinovirus humano muestra una ligera resistencia a los tratamientos, la selección natural puede promover la expansión de nuevas mutaciones, resultando en un fortalecimiento de esa resistencia.
Pese a la desalentadora variedad de rinovirus, algunos científicos siguen confiando en hallar una cura para el resfriado común. El hecho de que todas las cepas de rinovirus humano compartan un núcleo de genes sugiere que el núcleo no puede llevar a cabo mutaciones. Si los científicos encuentran el modo de atacar el núcleo genético del rinovirus, quizá sean capaces de frenar la enfermedad. Un prometedor punto débil en el núcleo del rinovirus es una franja de material genético que se dobla hasta formar un bucle con aspecto de hoja de trébol. La totalidad de los rinovirus que han estudiado los científicos presentan esta estructura de hoja de trébol. Todo apunta a que resulta esencial a la hora de acelerar el ritmo al que una célula huésped realiza copias de los genes del rinovirus. En el caso de que los científicos averigüen el modo de inutilizar la hoja de trébol, quizá neutralicen el conjunto de los virus del resfriado que circulan por la Tierra.
¿Pero deberían aspirar a ello? La respuesta no está clara. El rinovirus humano supone una carga muy onerosa para la salud pública no solo como causante de los resfriados, sino porque despeja el camino a patógenos más nocivos. Sin embargo, los efectos del rinovirus humano propiamente dicho son relativamente inocuos. La mayoría de los resfriados llegan a su fin en menos de una semana, y el 40 por ciento de las personas que dan positivo en las pruebas de rinovirus no muestra ningún síntoma. De hecho, el rinovirus humano puede ser útil para algunos de sus huéspedes humanos. Los científicos han reunido abundantes pruebas de que los niños que enferman a manos de virus y bacterias relativamente inofensivos pueden quedar protegidos frente a futuros trastornos inmunitarios, como alergias o la enfermedad de Crohn. Los rinovirus humanos pueden enseñar a nuestros sistemas inmunitarios a no reaccionar de forma exagerada frente a amenazas menores, reservando sus esfuerzos para las verdaderas amenazas.
Quizá no debamos considerar los virus como enemigos ancestrales, sino como viejos y sabios mentores.
Mirando hacia abajo desde las estrellas
La reinvención interminable de la gripe, Influenza (Término inglés para la gripe).
Si cierras los ojos y pronuncias la palabra en voz alta, suena encantadora. Le iría que ni pintado a un agradable e histórico pueblecito italiano. De hecho, la etimología de influenza es italiana (significa «influencia»). Su origen se remonta a la Edad Media. Pero las bellas asociaciones se detienen aquí. Los médicos medievales creían que las estrellas influían en la salud de sus pacientes, causando unas fiebres misteriosas que barrían Europa cada pocas décadas.
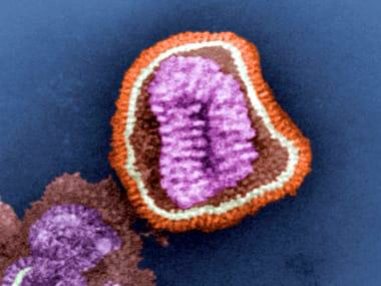
Virus de la gripe: la capa exterior es naranja mientras que la cápside es de un blanco grisáceo, con segmentos lilas de ARN en su interior
La gripe ha seguido causando devastaciones periódicas en el mundo. En 1918, un brote particularmente virulento de la gripe infectó a quinientos millones de personas —un tercio de la humanidad en aquel momento—, y se calcula que mató a cincuenta millones de ellas. Incluso en los años en que no se produce una epidemia, el peaje de la gripe es brutal. La Organización Mundial de la Salud (OMS) calcula que cada año la gripe infecta a entre un 5 por ciento y un 10 por ciento de todos los adultos, y a entre un 20 por ciento y un 30 por ciento de todos los niños. Entre 250.000 y 500.000 personas mueren anualmente por su culpa.
Los científicos saben hoy que la gripe no cae del cielo, sino que es obra de un virus microscópico. A imagen del rinovirus, responsable del resfriado, el virus de la gripe se las ingenia para infligir daño con muy escasa información genética, apenas trece genes. Estos se esparcen a partir de las gotitas que liberan los enfermos al toser o estornudar y por medio de sus narices goteantes. Una nueva víctima puede contraerla de forma accidental al inhalar una gotita portadora del virus o al tocar el pomo de una puerta y luego llevarse los dedos contaminados a la boca. Una vez el virus de la gripe penetra por la nariz o la garganta, puede acoplarse a una célula adherida a las vías respiratorias y colarse dentro. A medida que el virus de la gripe salta de una célula a otra a lo largo de las vías respiratorias, provoca el caos a su paso. La mucosidad y las células alineadas a lo largo de las vías respiratorias son destruidas como si el virus de la gripe fuera un cortacésped deslizándose por la hierba.
Cuando las personas sanas acaban infectadas con el virus de la gripe, sus sistemas inmunitarios pueden lanzar una contraofensiva en cuestión de días. Cuando esto ocurre, la gripe provoca una oleada de dolor, fiebre y fatiga, pero lo peor ha pasado en una semana. En un reducido porcentaje de víctimas, el virus despeja el camino para infecciones más serias. Por lo general, la capa superior de la célula sirve de barrera contra una amplia variedad de patógenos. Los patógenos se ven atrapados en la mucosidad y las células los agarran por medio de pelos, notificando de inmediato al sistema inmunitario la presencia de intrusos. Una vez el cortacésped de la gripe ha arrancado esta capa protectora, los patógenos pueden escurrirse dentro y causar graves infecciones pulmonares, algunas de ellas fatales.
Los virólogos siguen sin comprender algunas de las paradojas que plantean los efectos de la gripe. Las gripes estacionales son más peligrosas para aquellos individuos con sistemas inmunitarios débiles —en especial los niños y los ancianos —, porque son incapaces de mantener el virus a raya. Durante el brote de 1918, sin embargo, fueron los adultos jóvenes —los poseedores de sistemas inmunitarios fuertes— los que demostraron ser más vulnerables. Una teoría sostiene que determinadas cepas de la gripe provocan una respuesta tan agresiva del sistema inmunitario que acaba arrasando con el huésped en vez de barriendo el virus. Otros científicos cuestionan esta explicación y apuestan por buscar la respuesta en otro lado. Es posible, por ejemplo, que en 1918 la gente mayor fuera portadora de anticuerpos protectores a resultas de una pandemia similar acontecida en 1889.
Aunque los efectos de la gripe conservan su misterio, los orígenes son sobradamente conocidos. Se remontan a las aves. Las aves son portadoras de todas las cepas conocidas del virus de la gripe humana, junto con una inmensa variedad de otros virus de la gripe que no infectan a las personas. Muchas aves son portadoras de la gripe sin llegar a enfermar. En vez de infectar sus vías respiratorias, el virus de la gripe acostumbra a infectar sus intestinos. Como consecuencia, el virus es desechado a través de los excrementos. Las aves sanas que ingieren agua que lleva el virus contraen la enfermedad. En ocasiones, una cepa de gripe aviar se transmite a las personas. Puede que a través de un trabajador en una granja de pollos o en un puesto de carne en un mercado. Que un virus de la gripe aviar acabe en las vías respiratorias de un ser humano puede parecer extraño, pero resulta que los receptores de las células en las entrañas de las aves presentan una forma similar a la de los receptores celulares de nuestras vías respiratorias. Los virus de la gripe aviar pueden a veces adherirse a esos receptores y colarse dentro.
De todos modos, la transmisión de ave a persona no es sencilla. Los genes que un virus de la gripe aviar necesita para desarrollarse son diferentes de aquellos que requiere el interior del cuerpo humano. El cuerpo humano es más frío que el de las aves, por ejemplo, una diferencia que provoca que las moléculas necesiten formas distintas para progresar con eficiencia.
En consecuencia, los virus de la gripe aviar que saltan a los humanos acostumbran a chocar con un muro, ya que se ven incapacitados para moverse de un individuo a otro. En 2005, por ejemplo, una cepa de gripe procedente de las aves, llamada H5N1, provocó que centenares de personas comenzaran a enfermar en el Sudeste Asiático. Demostró ser mucho más mortífera que las cepas de la gripe estacionales, por lo que los responsables de la salud pública siguieron su evolución con detenimiento, adoptando medidas para contener su expansión. Pero año sí, año también, se reveló incapaz de pasar de una persona a otra. Los virus H5N1 que penetran en los seres humanos siempre acaban muriendo, bien porque sus huéspedes los destruyen, bien porque ellos mismos matan a sus huéspedes.
De vez en cuando, sin embargo, los virus de la gripe aviar se adaptan a nuestros cuerpos. Cada vez que se replican, los nuevos virus contienen errores genéticos conocidos como mutaciones. Algunas de estas mutaciones no tienen efecto alguno sobre los virus. Algunas los inhabilitan de cara a su reproducción. Pero unas pocas conceden una ventaja reproductiva a los virus de la gripe. La selección natural favorece estas mutaciones beneficiosas. Algunas ayudan al virus alterando la forma de las proteínas que recubren su cáscara, facilitándoles la labor de agarrar células humanas. Otras lo ayudan a difundirse de una persona a otra.
Desde el momento en que una cepa de la gripe arraiga en los humanos, puede propagarse por el mundo y empezar a expandirse y contraerse de forma estacional. En lugares como Estados Unidos, la mayoría de las gripes ocurren en invierno. Una hipótesis sostiene que se debe a que, en esos meses, el aire está tan seco que permite a las gotitas que acarrean el virus permanecer en el aire durante varias horas, multiplicando sus probabilidades de hallar un nuevo huésped. En otros periodos del año, la humedad lleva a las gotitas a hincharse y caer al suelo. Cuando un virus de la gripe se monta en una gotita e infecta un nuevo huésped, a veces invade una célula que ya acoge a otro virus de la gripe. Y cuando dos virus de la gripe diferentes se reproducen en el interior de una misma célula, las cosas pueden ponerse feas. Los genes de un virus de la gripe se almacenan en ocho segmentos separados y, en el momento en que una célula huésped comienza a fabricar segmentos de dos virus distintos de manera simultánea, en ocasiones acaban mezclados. La descendencia resultante es portadora de material genético de ambos virus. Esta combinación, llamada intercambio, es la versión viral del sexo. Cuando los seres humanos tienen hijos, los genes de ambos progenitores se mezclan, creando nuevas combinaciones a partir de los dos juegos de ADN. El intercambio permite a los virus de la gripe una mezcolanza de genes para alumbrar nuevas combinaciones propias.
Una cuarta parte de las aves con gripe llevan en su interior dos o más cepas del virus. Los virus intercambian genes y obtienen nuevas adaptaciones, como la habilidad de pasar de vivir entre aves salvajes a hacerlo entre pollos, o incluso entre mamíferos como cerdos y caballos. En muy raras ocasiones, el intercambio resulta en combinaciones de genes de aves y humanos, lo que supone una receta para el desastre. La nueva cepa salida de esta combinación puede saltar con facilidad de una persona a otra. Y puesto que es la primera vez que circula entre los humanos, nadie posee las defensas susceptibles de frenar la expansión de la cepa nueva.
Una vez los virus de la gripe aviar evolucionan hasta dar paso a patógenos humanos, siguen intercambiando genes entre ellos. Este intercambio sostenido permite a los virus sortear la destrucción. Antes de que los sistemas inmunitarios de las personas se familiaricen en exceso con las proteínas en la superficie de una cepa de la gripe, pueden recurrir a un poco de sexo viral de cara a adoptar un nuevo disfraz. El papel jugado por el intercambio en una reciente pandemia resultó especialmente complejo. La cepa nueva, llamada humano-porcina, surgió por primera vez en México en marzo de 2009. Su gestación, sin embargo, requirió de décadas.
Al secuenciar sus genes, los científicos han remontado los orígenes del virus hasta cuatro cepas diferenciadas. La más antigua lleva infectando a cerdos desde la pandemia de 1918 (es posible que los cerdos la adquirieran de nosotros). Una segunda cepa emergió en la década de 1970, cuando una gripe aviar infectó a cerdos en Europa o Asia. Y una tercera saltó de las aves a los cerdos en Estados Unidos. A finales de la década de 1990, las tres cepas se habían combinado hasta adquirir una forma nueva, a la que los científicos bautizaron como triple intercambio. Sin que fuera percibido en su momento, fue pasando de forma sigilosa entre cerdos confinados en granjas de grandes dimensiones. A continuación, el triple intercambio se mezcló con otros virus de la gripe porcina y de aquí pudo saltar a los seres humanos. Es probable que el H1N1 humano-porcino de 2009 realizara el salto en el otoño de 2008 y fuera enfermando a la gente durante meses, hasta visibilizarse en la primavera de 2009.
Tan pronto los responsables de la salud pública tomaron conciencia de que tenían una pandemia entre manos, lanzaron una campaña global para proteger a la gente de la infección. Pese a sus esfuerzos, el H1N1 humano-porcino de 2009 fue capaz de expandirse por todo el planeta, como las pandemias que lo precedieron, infectando a entre un 10 por ciento y un 20 por ciento de la población mundial. Estados Unidos se apresuró a producir una nueva vacuna para el H1N1 humano-porcino de 2009, pero no estuvo lista hasta el otoño y finalmente solo ofreció una protección moderada contra el virus.
Si el H1N1 humano-porcino de 2009 hubiera sido tan letal como la gripe de 1918, podríamos habernos enfrentado a otra catástrofe gigantesca, con un saldo de millones de muertos. A la postre se reveló leve, causando 250.000 muertes antes de evaporarse. Mientras escribo esto, a lo largo del año 2015, los científicos intentan adelantarse a las próximas pandemias. Quizá basten unas pocas mutaciones para que una cepa de gripe aviar evolucione hasta convertirse en una nueva cepa de virus humano de la gripe. Los intercambios podrían acelerar los cambios. Nadie es capaz de predecir cuándo ni si una cepa en particular llevará a cabo el salto. Sin embargo, mientras aguardamos a lo que la evolución nos tiene reservado, no estamos indefensos. Contamos con recursos para ralentizar la expansión de la gripe, como lavarnos las manos.
Asimismo, los científicos están aprendiendo a fabricar vacunas más efectivas siguiéndole el rastro a la evolución del virus de la gripe, lo que permitirá predecir mejor las cepas que acarrearán un mayor peligro en las futuras temporadas de gripe. Puede que aún no le hayamos tomado la delantera a la gripe, pero, al menos, ya no tenemos que mirar a las estrellas en busca de protección.
Conejos con cuernos
El virus del papiloma humano y el cáncer infeccioso
Durante siglos circularon historias sobre conejos con cuernos. Con el tiempo cristalizaron en el mito del lebrílope. Si visitas Wyoming y acabas buscando postales del lugar, es muy probable que te topes con una foto de un lebrílope dando saltos por la pradera. Su aspecto es el de un conejo al que le sobresalen un par de astas. Quizá hasta te cruces con un ejemplar de carne y hueso, por lo menos con la cabeza de uno decorando la pared de un restaurante.
Por un lado, todo es una patraña. La mayoría de los lebrílopes no son más que un engaño taxidérmico, es decir, conejos con trozos de asta de antílope pegados a la cabeza. Pero, como tantos mitos, la historia del lebrílope contiene una semilla de verdad enterrada en su interior. A algunos conejos, en efecto, les salen protuberancias en la cabeza.
A principios de la década de 1930, Richard Shope, un científico de la Universidad Rockefeller, oyó hablar de conejos con cuernos durante una cacería. Consiguió que un amigo cazara uno y le enviara tejido de los cuernos para averiguar su composición. Un colega de Shope, Francis Rous, había realizado experimentos con pollos que sugerían que los virus eran capaces de causar tumores. Muchos científicos se mostraron escépticos en aquel momento, pero Shope se preguntó si detrás de los «cuernos» de los conejos no habría también tumores, provocados de alguna manera por un virus desconocido. Para someter a prueba su hipótesis, Shope molió los fragmentos de cuerno, los mezcló en una solución y filtró el líquido echando mano de la porcelana. Los poros finos de la porcelana solo permitirían el paso a los virus. A continuación Shope frotó la solución filtrada en la cabeza de conejos sanos. También les crecieron cuernos.
El experimento de Shope fue más allá de demostrar que los cuernos contenían virus. Reveló que los virus creaban los cuernos, moldeándolos a partir de células infectadas. Tras este descubrimiento, Shope entregó su colección de tejidos de conejo a Rous, quien continuó trabajando con ella durante décadas. Rous inyectó líquido repleto de virus en las entrañas de los conejos y comprobó que no provocaba que les salieran inofensivos cuernos. En vez de esto, los conejos desarrollaban cánceres agresivos que los mataban. Por sus investigaciones en las que vinculaba virus y cánceres, Rous obtuvo el Premio Nobel de Medicina en 1966.
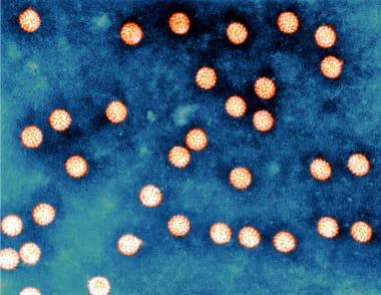
El virus del papiloma humano (VPH) en suspensión
Los descubrimientos de Shope y Rous impulsaron a los científicos a estudiar los tumores en otros animales. Las vacas desarrollan ocasionalmente bultos monstruosos de piel deforme que alcanzan el tamaño de pomelos. A mamíferos como los delfines, los tigres o los humanos les salen verrugas. Y de forma muy excepcional brotan verrugas susceptibles de convertir a una persona en un lebrílope.
En la década de 1980, a un adolescente de Indonesia llamado Dede empezaron a salirle verrugas que no tardaron en cubrirle por completo manos y pies. Con el tiempo se vio incapacitado para trabajar y acabó formando parte de un circo de rarezas, recibiendo el apodo de «el hombre árbol». La prensa comenzó a hacerse eco del caso de Dede y, en 2007, los médicos le extrajeron casi treinta kilos de verrugas del cuerpo. Debido a la reaparición ocasional de las verrugas, Dede tuvo que someterse a nuevas cirugías. Los tumores de Dede, junto a los del resto de los mamíferos y animales, fueron resultado de un único virus, el mismo que hizo que a los conejos les salieran cuernos. Se le conoce con el nombre de virus del papiloma, por la papila (del latín, «botón») que forman las células infectadas.
En la década de 1970, el investigador alemán Harald zur Hausen especuló con la posibilidad de que el virus del papiloma supusiera un riesgo para la salud de las personas que fuera mucho más allá de una simple verruga ocasional. Se preguntó si podría provocar tumores en el cuello del útero. Estudios previos en casos de cáncer cervical revelaron patrones similares a los de enfermedades de transmisión sexual. Las monjas, por ejemplo, padecen cáncer cervical en proporciones mucho menores que el resto de las mujeres. Algunos científicos habían planteado la posibilidad de que un virus liberado durante la práctica del sexo estuviera detrás del cáncer cervical. Zur Hausen se preguntó si no se trataría del virus del papiloma.
Zur Hausen concluyó que, de ser esto cierto, debería encontrar ADN del virus en los tumores cervicales. Recopiló biopsias para su estudio y se dedicó con paciencia a analizar su ADN durante años. En 1983, descubrió material genético del virus del papiloma en las muestras. A medida que prosiguió con el análisis de las biopsias, se le fueron presentando más cepas del papiloma. Desde que Zur Hausen publicara por primera vez sus hallazgos, los científicos han identificado más de un centenar de cepas diferentes del virus del papiloma humano (VPH para abreviar). Zur Hausen compartió el Premio Nobel de Medicina en 2008 por sus esfuerzos.
Los estudios de Zur Hausen colocaron el virus del papiloma humano bajo el foco médico debido al pavoroso número de muertes que el cáncer cervical provoca entre las mujeres de todo el mundo. Los tumores causados por el VPH alcanzan tal tamaño que en ocasiones llegan a desgarrar el útero o los intestinos. El sangrado resultante puede devenir fatal. El cáncer cervical se cobra anualmente más de 270.000 vidas, lo que supone la tercera causa de defunción entre la población femenina, superado únicamente por el cáncer de pecho y el cáncer de pulmón.
Todos los casos empiezan con una infección de VPH. La infección se produce cuando un virus inyecta su ADN en una célula huésped. El VPH se especializa en la infección de las células epiteliales, las cuales conforman buena parte de las membranas mucosas de la piel y del cuerpo. Los genes del virus acaban en el interior del núcleo de su célula huésped, el hogar del ADN de la propia célula. A continuación la célula lee los genes del VPH y fabrica las proteínas del virus. Estas proteínas empiezan a alterar la célula. Muchos otros virus, como el rinovirus o el virus de la gripe, se reproducen de forma agresiva. Fabrican nuevos virus a la máxima velocidad posible, hasta que la célula huésped rebosa de descendencia viral. En última instancia, la célula se desgarra y muere. El VPH recurre a una estrategia completamente distinta. En vez de matar a su célula huésped, fuerza a que la célula ejecute más copias de sí misma. Cuanto mayor sea el número de células huésped, mayor será el número de virus.
Acelerar la división de una célula no es un logro menor, sobre todo para un virus dotado de solo ocho genes. El proceso habitual de división celular es de una complejidad mayúscula. Una célula decide dividirse en respuesta a señales tanto del interior como del exterior, movilizando a un ejército de moléculas para reorganizar su contenido. Su esqueleto interno de filamentos se ensambla de nuevo, desgajando los contenidos de la célula y llevándolos hasta dos extremos. Al mismo tiempo, la célula realiza una nueva copia de su ADN, 3.200 millones de letras en total, organizadas en cuarenta y seis agrupaciones llamadas cromosomas. La célula debe arrastrar estos cromosomas hasta ambos extremos de sí misma y levantar un muro en el centro.
Durante este frenesí de actividad, unas moléculas supervisoras se dedican a hacer un seguimiento del progreso. Si la célula da señales de convertirse en cancerosa, pueden forzarla a suicidarse. El VPH es capaz de manipular esta danza compleja fabricando unas pocas proteínas que intervengan en momentos críticos del ciclo de la célula, acelerándolo sin llegar a matarla. Muchas células crecen con rapidez durante la infancia para ralentizar el proceso o detenerlo más adelante. Las células epiteliales, aquellas a las que infecta el VPH, siguen creciendo a lo largo de toda nuestra vida. Comienzan en una capa que se halla enterrada bajo la superficie cutánea. A medida que se dividen, fabrican una capa de células nuevas que empujan a las que tienen por encima. En el proceso de dividirse y empujar hacia arriba, las células van diferenciándose de sus progenitores. Empiezan a producir una proteína muy dura llamada queratina (la misma sustancia de la que están hechas las uñas y las pezuñas de los caballos). Repleta de queratina, la capa superior de la piel puede soportar mejor los estragos causados por el sol, las sustancias químicas y las temperaturas extremas. Con el tiempo, la capa superior de las células epiteliales muere para dar paso a la siguiente capa de células epiteliales.
Esta situación implica que el VPH debe intentar subsistir en una cinta transportadora. A medida que las células infectadas de VPH se reproducen, van desplazándose hacia arriba y acercándose progresivamente a su muerte. Los virus perciben el momento en que sus células huésped se aproximan a la superficie y cambian de estrategia. En vez de acelerar la división celular, ordenan a las células huésped que fabriquen un gran número de virus nuevos. Cuando la célula alcanza la superficie, explosiona con una carga abundante de VPH que puede salir a la búsqueda de nuevos huéspedes a los que infectar.
La mayoría de las personas infectadas con VPH experimentan un calmado equilibrio entre el virus y el huésped. Las células infectadas que crecen a un ritmo alto no causan daño porque acaban eliminadas. Mientras tanto, el virus recurre a las células epiteliales como fábrica de nuevos virus, susceptibles luego de infectar a nuevos huéspedes por medio del contacto piel con piel o de las relaciones sexuales. El sistema inmunitario ayuda a mantener el equilibrio desembarazándose de algunas de las células infectadas. (Los tumores de forma arborescente de Dede fueron resultado de un defecto genético que inhabilitaba a su cuerpo para someter al virus). Este equilibrio entre huésped y virus lleva en marcha desde hace cientos de millones de años. Para reconstruir la historia del virus del papiloma, los científicos comparan la secuencia genética de diferentes cepas y toman nota de los animales infectados. Resulta que el virus del papiloma no solo infecta a los mamíferos, como es el caso de los humanos, los conejos o las vacas, sino también a otros vertebrados, como las aves y los reptiles. Cada cepa del virus acostumbra a infectar a una única especie o a unas pocas especies relacionadas entre sí.
Atendiendo a estas relaciones, Marc Gottschling, de la Universidad de Múnich, ha argumentado que los primeros vertebrados terrestres que depositaron huevos — los ancestros de los mamíferos, aves y reptiles— ya actuaron como huéspedes del virus del papiloma, hace trescientos millones de años. A medida que los descendientes de esos animales tan remotos fueron evolucionando en diversos linajes, sus virus del papiloma hicieron lo propio. Algunos estudios sugieren que estos virus comenzaron a especializarse en diferentes partes de sus huéspedes. Los virus que causan las verrugas, por ejemplo, se adaptaron para infectar las células epidérmicas. Hubo los que se adaptaron a las hileras de mucosas de la boca y a otros orificios. Por lo general, estos nuevos virus del papiloma coexistieron de manera pacífica con sus huéspedes. Dos tercios de los caballos sanos son portadores de cepas del virus del papiloma llamadas BPV1 y BPV2. Algunas cepas evolucionaron hasta ser más propensas a resultar cancerígenas que otras, algo para lo que los investigadores carecen de explicación.
A lo largo de miles de generaciones, los virus del papiloma se han especializado en determinados huéspedes, pero, de forma ocasional, también han saltado a otras especies. Un puñado de virus del papiloma humano mantienen una relación más estrecha con virus del papiloma que infectan a animales de los que estamos alejados, por ejemplo, los caballos, que con virus del papiloma de parientes más cercanos a nosotros, como es el caso de los simios. Quizá bastó un contacto a nivel cutáneo para que se produjera el salto.
Cuando nuestra especie comenzó a evolucionar en África, unos doscientos mil años atrás, es probable que nuestros ancestros fueran portadores de diversas cepas del virus del papiloma. Representantes de aquellas cepas campan hoy por todo el mundo. Pero a medida que los seres humanos se expandieron a lo largo y ancho del planeta —abandonando África hace unos cincuenta mil años y alcanzando el Nuevo Mundo hace unos quince mil—, sus virus del papiloma no dejaron de evolucionar. Lo sabemos porque la genealogía de algunas cepas del VPH refleja la genealogía de nuestra especie. Los virus que hoy infectan a los africanos, por ejemplo, se remontan a los linajes más antiguos del VPH, mientras que los europeos, los asiáticos y los nativos americanos son portadores de sus propias cepas diferenciadas.
Solo durante cincuenta de los últimos doscientos mil años, nuestra especie ha sido consciente de ser portadora del virus del papiloma humano. Esto no es atribuible a la rareza del VPH, pues un estudio realizado en 2013 a ciento tres personas sanas detectó que setenta y una de ellas eran portadoras, es decir, un 69 por ciento. Para una mayoría abrumadora de aquellos individuos la experiencia resultó inofensiva. De los treinta millones de mujeres estadounidenses que se estima que son portadoras del VPH, solo trece mil desarrollan anualmente un cáncer cervical. En esta minoría afectada por el cáncer, el equilibrio armonioso entre huésped y virus desaparece. Natalia Shulzhenko, de la Universidad Estatal de Oregón, y sus colegas de laboratorio han postulado que el VPH activa el cáncer cuando parte de su material genético se ve accidentalmente incorporado al ADN de una célula. La célula se multiplica a gran velocidad y efectúa nuevas mutaciones. En vez de morir, permanece en un estado anormalmente joven. En vez de ser descartadas, las células forman un tumor que empuja hacia fuera y penetra en el tejido circundante.
La forma más eficaz de prevenir la mayoría de los cánceres es reducir las probabilidades de que nuestras células ejecuten mutaciones peligrosas: dejar de fumar, evitar las sustancias químicas que favorecen los cánceres y llevar una alimentación sana. Sin embargo, existe otra manera de bloquear el cáncer cervical: por medio de una vacuna. En 2006, Estados Unidos y Europa dieron luz verde a la aplicación de las primeras vacunas contra el VPH. Todas ellas contienen proteínas procedentes de la cáscara exterior del VPH, que el sistema inmunitario puede aprender a reconocer. Si más adelante las personas caen infectadas con el VPH, sus sistemas inmunitarios son capaces de organizar una contraofensiva rápida y eliminarlo.
La introducción de la vacuna desató la controversia en Estados Unidos porque el fabricante, GlaxoSmithKline, recomendó vacunar a los niños de entre once y trece años. Algunos padres alegaron que semejante política alentaba el sexo antes del matrimonio. La polémica hizo que los índices de vacunación fueran bajos. En 2013, solo el 35 por ciento de los chicos y el 57 por ciento de las chicas habían recibido la vacuna del VPH al llegar a los trece años. Los Centros para el Control y la Prevención de Enfermedades (CDC) lamentaron que estos porcentajes fueran «inaceptablemente pobres».
Con independencia de las reservas que los padres muestren hacia la vacuna, su efectividad está fuera de duda. Estudios a largo plazo han demostrado que garantiza una protección total contra las dos principales cepas que hay detrás del 70 por ciento de los casos de cáncer cervical. Pero ni siquiera el hecho de que todos los niños llegaran a recibir la vacuna garantizaría la desaparición del cáncer cervical. En el mejor de los casos, se erradicarían las dos cepas sobre las que actuaría la vacuna. Y es que los científicos han identificado otras trece cepas del VPH susceptibles de provocar un cáncer, y muy probablemente queden otras por descubrir. Si las vacunas borraran del mapa las dos cepas más exitosas, la selección natural bien podría favorecer la evolución de otras cepas para que ocuparan su lugar. Jamás se debería subestimar la creatividad evolutiva de un virus capaz de convertir a conejos en lebrílopes, o a hombres en árboles.
El enemigo de nuestro enemigo
Los bacteriófagos como medicina viral
A principios del siglo XX, los científicos ya habían aprendido varias cosas relevantes acerca de los virus. Sabían que eran agentes infecciosos de un tamaño asombrosamente pequeño. Sabían que determinados virus causaban determinadas enfermedades, como era el caso de la enfermedad del mosaico del tabaco o de la rabia. Sin embargo, la joven ciencia de la virología seguía muy acotada. Se centraba principalmente en aquellos virus que más preocupaban a la gente: los que les provocaban enfermedades, los que amenazaban a sus cosechas y a su ganado. Los virólogos raramente miraban más allá de nuestro limitado círculo de experiencias. Hubo que esperar a la Primera Guerra Mundial para que dos médicos, de manera independiente, vislumbraran el universo expandido de virus en el que vivimos.
En 1915, un médico británico llamado Frederick Twort se topó con este universo por accidente. En aquel momento su objetivo era simplificar la fabricación de vacunas para la viruela. A principios del siglo XX, la vacuna estándar para esta enfermedad contenía un pariente más benigno de la viruela, llamado virus vacuna. Por desgracia los nuevos virus vacuna solo podían obtenerse de los huéspedes: bien de seres humanos inmunizados, bien de animales inmunizados. Twort se preguntó si podría conseguirse que el virus vacuna creciera más rápido a base de infectar células que cultivaba en las placas de su laboratorio.
Sus experimentos fracasaron, ya que las bacterias acabaron contaminando las placas y matando las células. La frustración de Twort no impidió que reparara en algo extraño. Detectó unos puntos cristalinos formándose en las placas. Bajo el microscopio observó que los puntos rebosaban de microbios muertos. Extrajo unas gotitas de estos puntos y las transfirió a colonias de bacterias vivas. En cuestión de horas, se formaron puntos cristalinos en las placas nuevas, que se llenaron de más bacterias muertas. Pero comprobó que si vertía gotitas sobre una especie de bacteria diferente, no se formaban puntos.
A Twort se le ocurrieron tres explicaciones para lo que estaba presenciando. Quizá se tratara de una cualidad extraña del ciclo vital de la bacteria. O puede que las bacterias estuvieran fabricando algunas enzimas que las mataban. La tercera posibilidad era la más difícil de concebir: puede que hubiera descubierto un virus capaz de matar a las bacterias. Twort publicó sus hallazgos, expuso las tres posibilidades y dejó reposar el asunto. Al parecer, una idea tan radical como la de unos virus infectando a una bacteria no llegó a infectar su mente. Ahora bien, cuando dos años después un médico canadiense llamado Félix d’Herelle realizó el mismo descubrimiento por su cuenta, su resistencia se aplacó.
En 1917, D’Herelle trabajaba como médico militar, atendiendo a soldados franceses que morían de disentería. La causa de la disentería yace en una bacteria denominada Shigella. Hoy en día los médicos recurren a los antibióticos para matar a las bacterias, pero no serían descubiertos hasta varias décadas después de la Primera Guerra Mundial. De cara a tener un conocimiento más profundo de su enemigo, D’Herelle examinó la diarrea de los soldados enfermos. Como parte de su análisis, se dedicó a pasar las heces por filtros muy finos, atrapando a la Shigella y a cualquier otra bacteria que contuvieran. Una vez obtenido este filtro depurado y libre de bacterias, D’Herelle lo mezcló con una muestra reciente de Shigella y extendió la combinación de bacterias y fluido depurado por placas de Petri. La Shigella empezó a crecer, pero, al cabo de pocas horas, D’Herelle advirtió cómo empezaban a formarse unos puntos claros en sus colonias. Acto seguido extrajo muestras de estos puntos y las volvió a mezclar con Shigella. En las placas surgieron nuevos puntos claros. D’Herelle concluyó que estos puntos eran campos de batalla en los que los virus mataban a la Shigella y dejaban atrás sus cadáveres translúcidos.
Convencido de la radicalidad de su descubrimiento, D’Herelle pensó que sus virus merecían un nombre propio. Los bautizó como bacteriófagos, cuyo significado es «comedores de bacterias». Hoy se los conoce con la abreviatura fagos. La idea de una bacteria infectando a un virus sonaba tan rara que algunos científicos la desecharon. Jules Bordet, un médico inmunólogo francés que ganó el Premio Nobel en 1919, se erigió en el mayor opositor público a D’Herelle al mostrarse incapaz de hallar fagos. En vez de a la Shigella, Bordet recurrió a una cepa inofensiva de Escherichia coli. Pasó líquido lleno de E. coli por unos filtros finos y mezcló el líquido filtrado con una segunda tanda de E. coli. Igual que ocurriera con los experimentos de D’Herelle, esta segunda tanda murió. Bordet decidió entonces comprobar qué ocurría si mezclaba el líquido filtrado con la primera tanda de E. coli, es decir, con la que había filtrado en primer lugar. Para su sorpresa, la primera tanda de E. coli se reveló inmune.
Bordet estaba convencido de que su fracaso a la hora de matar a la bacteria significaba que el fluido filtrado no contenía fagos. Pensó que en su lugar contenía una proteína fabricada por el primer E. coli. La proteína se mostraba tóxica con otras bacterias, pero no con aquellas que la habían creado. D’Herelle plantó cara a Bordet, Bordet contraatacó y el debate estuvo años encendido. No fue hasta la década de 1940 que los científicos al fin dieron con las pruebas visuales que otorgaban la razón a D’Herelle. La polémica solo se zanjó gracias a la invención de unos microscopios electrónicos dotados de la potencia suficiente para observar virus minúsculos. Al mezclar el fluido capaz de matar a las bacterias con E. coli y colocar el resultado bajo el microscopio, vieron a los fagos atacar a las bacterias. Los fagos poseían unos caparazones en forma de caja, donde sus genes aparecían enroscados y montados sobre lo que se asemejaba a un conjunto de patas de araña. Los fagos descendían sobre la superficie del E. coli, al modo de un módulo espacial sobre la luna, y a continuación perforaban el microbio y rociaban su ADN por el interior.
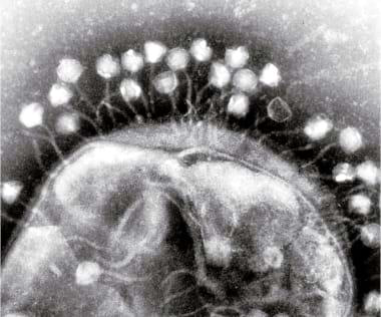
Bacteriófagos adheridos a la superficie de una célula huésped, una bacteria Escherichia coli
A medida que los científicos fueron familiarizándose con los fagos, quedó en evidencia que la trifulca entre D’Herelle y Bordet fue como mezclar churras con merinas. Los fagos no pertenecen a una sola especie, y diferentes especies de fagos se comportan de modos distintos con sus huéspedes. D’Herelle había descubierto una forma muy virulenta, llamada fago lítico, que mata a su huésped a medida que se multiplica. Bordet había descubierto una forma más benigna de virus, llamada fago moderado. Los fagos moderados tratan a las bacterias de un modo muy parecido a como el virus del papiloma humano trata a nuestras células cutáneas. Cuando un fago moderado infecta a su microbio huésped, su huésped no eclosiona liberando nuevos fagos. En vez de esto, los genes del fago moderado son adheridos al ADN del propio huésped y el huésped continúa creciendo y dividiéndose. Es como si el virus y su huésped se fusionaran en uno solo.
De todos modos, cada cierto tiempo el ADN del fago moderado se despierta y ordena a la célula que fabrique fagos nuevos, los cuales brotan con fuerza de la célula e invaden otras nuevas. Y una vez el fago moderado se incorpora al interior de un microbio, el huésped se vuelve inmune ante invasiones futuras. Esto explica que Bordet no pudiera matar a su primera tanda de E. coli con el fago, pues ya estaba infectada y, por lo tanto, protegida. D’Herelle no esperó a que se cerrara el debate sobre los fagos para empezar a utilizarlos para curar a sus pacientes. Durante la Primera Guerra Mundial había observado que a medida que los soldados se recuperaban de la disentería y de otras enfermedades, los niveles de fagos presentes en sus heces se disparaban. D’Herelle llegó a la conclusión de que los fagos mataban a las bacterias. Por tanto, si ofrecía a los soldados una dosis extra de fagos, quizá acelerara su curación.
Antes de someter a prueba esta hipótesis, D’Herelle debía asegurarse de que los fagos no fueran nocivos. De modo que ingirió algunos para comprobar si enfermaba. Más tarde escribió que era capaz de tragar fagos «sin detectar la menor señal de malestar». D’Herelle se inyectó fagos en la piel con idéntico resultado. Convencido de su benignidad, empezó a ofrecérselos a sus pacientes enfermos. D’Herelle informó de que ayudaban a la gente a reponerse de la disentería y del cólera. Cuando cuatro pasajeros a bordo de una embarcación francesa en el canal de Suez cayeron enfermos de peste bubónica, les dio fagos. Todos ellos sanaron.
Los remedios de D’Herelle aumentaron todavía más su celebridad. En 1925, el escritor estadounidense Sinclair Lewis convirtió los estudios avanzados de D’Herelle en la base de su novela superventas Arrowsmith, que Hollywood llevó a la gran pantalla en 1931. En paralelo, D’Herelle elaboró medicamentos a partir de fagos que comercializó la empresa hoy conocida como L’Oreal. La gente recurría a sus fagos para tratar heridas en la piel y para curar infecciones intestinales.
Pero para 1940, la fiebre despertada por los fagos había llegado a su fin. La idea de emplear virus vivos como medicina había perturbado a muchos médicos. Cuando se descubrieron los antibióticos en la década de 1930, esos mismos médicos reaccionaron con mucho más entusiasmo, pues los antibióticos no estaban vivos; no eran más que sustancias químicas artificiales y proteínas fabricadas por hongos y bacterias. Además eran asombrosamente efectivos, con frecuencia eliminaban una infección en cuestión de días. Las compañías farmacéuticas dieron la espalda a los fagos de D’Herelle y se volcaron en la producción de antibióticos. Su éxito fue tal que acabó desmontando los argumentos a favor de proseguir investigando las terapias con fagos.
Sin embargo, el sueño de D’Herelle no se extinguió por completo a su muerte, ocurrida en 1949. Durante un viaje a la Unión Soviética en la década de 1920, había contactado con unos científicos deseosos de dedicar un centro de investigación al estudio exclusivo de las terapias con fagos. En 1923, ayudó a los investigadores soviéticos a abrir el Instituto Eliava de Bacteriofagia, Microbiología y Virología en Tiflis, capital de la actual República de Georgia. En su momento de máximo rendimiento, el instituto llegó a emplear a mil doscientas personas dedicadas a la producción de varias toneladas de fagos cada año.
Durante la Segunda Guerra Mundial, la Unión Soviética envió cargamentos de fago en polvo y en pastillas al frente para ser distribuidos entre sus soldados infectados. En 1963, el Instituto Eliava llevó a cabo el estudio más completo jamás visto con el objetivo de medir la eficacia real de los fagos en las personas, reclutando a 30.769 niños de Tiflis. Una vez a la semana, la mitad de ellos ingerían una pastilla que contenía fagos contra la Shigella. La otra mitad recibía una pastilla rellena de azúcar. Para reducir al mínimo los condicionantes ambientales, los científicos del Eliava repartieron las pastillas de fagos solo entre los niños que vivían en un mismo lado de la calle, y las pastillas de azúcar solo entre los niños que vivían en el lado opuesto. Los científicos hicieron un seguimiento de los niños durante ciento nueve días. Entre aquellos que ingirieron las pastillas de azúcar, 6,7 de cada mil contrajeron disentería. Entre aquellos que ingirieron las pastillas de fagos, la cifra se redujo a 1,8 de cada mil. En otras palabras, tomar fagos reducía en un 3,8 por ciento las probabilidades de que un niño enfermara.
El secretismo consustancial al Gobierno soviético impidió que unos resultados tan llamativos trascendieran más allá de Georgia. Solo el derrumbamiento de la Unión Soviética en 1989 permitió su filtración. Los informes han animado a un reducido pero combativo grupo de científicos occidentales a investigar la terapia con fagos, desafiando la reticencia a su uso que Occidente ha mostrado tradicionalmente. Estos defensores de los fagos sostienen que no deberíamos preocuparnos por utilizar virus vivos en los tratamientos médicos. A fin de cuentas, alimentos de consumo cotidiano como los yogures, los pepinillos o el salami contienen hordas de fagos. Nuestros cuerpos también acogen enormes reservas de ellos, lo que no es de extrañar si tenemos en cuenta que cada uno de nosotros acarrea cien billones de bacterias, todas ellas huéspedes más que prometedores para diversas especies de fagos. A diario estos fagos matan a cantidades enormes de bacterias dentro de nuestros cuerpos sin causar el menor perjuicio a la salud.
Otro motivo de preocupación despertado por los fagos es que su ataque resulta excesivamente focalizado. Cada especie de fago puede atacar a una única especie de bacteria, mientras que un antibiótico puede eliminar a varias especies al mismo tiempo. A estas alturas, sin embargo, está demostrado que la terapia con fagos es útil en el tratamiento de una amplia variedad de infecciones. Los médicos solo tienen que combinar diversas especies de fagos en un único cóctel. Los científicos del Instituto Eliava han desarrollado un apósito para heridas que está impregnado con seis fagos diferentes, el cual es capaz de matar a los seis tipos de bacterias más comunes en las infecciones de heridas cutáneas.
Los escépticos también han argumentado que incluso en el supuesto de que los científicos diseñaran una terapia con fagos eficaz, la evolución se encargaría de volverla inservible. En la década de 1940, los microbiólogos Salvador Luria y Max Delbrück fueron testigos directos de la resistencia mostrada por los fagos. Al llenar una placa de E. coli con fagos, la mayor parte de las bacterias murieron, pero un puñado se aferró a la existencia y luego se multiplicó hasta formar nuevas colonias. Estudios posteriores revelaron que las supervivientes habían adquirido mutaciones que las facultaron para resistir a los fagos. A continuación, las bacterias resistentes traspasaron sus genes mutados a su descendencia. Las voces críticas han señalado que la terapia con fagos promoverá la evolución de bacterias resistentes a los fagos, permitiendo el efecto rebote de las infecciones.
Los defensores de la terapia les responden que los fagos también son capaces de evolucionar. A medida que se replican, en ocasiones llevan a cabo mutaciones, algunas de las cuales les abren nuevos caminos para infectar bacterias resistentes. Los científicos pueden incluso ayudar a los fagos a mejorar sus ataques. Por ejemplo, explorando entre miles de grupos de fagos diferentes para dar con el arma más eficaz a la hora de combatir una infección en concreto. Su margen de acción llega hasta el extremo de ser capaces de manipular el ADN del fago para crear fagos susceptibles de matar de modos nunca vistos.
En 2008, James Collins, un biólogo de la Universidad de Boston, y Tim Lu, del Instituto Tecnológico de Massachusetts, publicaron detalles del primer fago programado para matar. Su nuevo fago es especialmente eficaz porque está diseñado para atacar a las matrices en las que las bacterias se embeben, llamadas biofilms. El biofilm puede neutralizar por igual a antibióticos y fagos, ya que estos no consiguen penetrar la mucosidad sólida y acceder a las bacterias del interior. Collins y Lu peinaron las publicaciones científicas a la búsqueda de un gen capaz de mejorar la letalidad de los fagos a la hora de destruir a los biofilms. Las propias bacterias acarrean enzimas a las que recurren para aflojar los biofilms cuando llega el momento de que se liberen y salgan flotando con el objetivo de colonizar nuevos hábitats.
Collins y Lu sintetizaron un gen para una de estas enzimas capaces de disolver biofilms y la insertaron en un fago. A continuación, modificaron el ADN del fago para que fabricara montones de enzimas tan pronto accediera al microbio huésped. Al descargarlo sobre biofilms de E. coli, los fagos penetraron en los microbios localizados en la parte superior de los biofilms y los forzaron a fabricar tanto nuevos fagos como nuevas enzimas. Los microbios infectados eclosionaron, liberando enzimas que abrieron capas más profundas de biofilms a las que los fagos podían ahora infectar. Los fagos de diseño pueden acabar con el 99,997 por ciento del E. coli de un biofilm, un porcentaje de letalidad que multiplica por cien la efectividad de los fagos normales.
Mientras Collins y otros científicos estudian modos de aumentar la eficacia de los fagos, los antibióticos están perdiendo parte de su buena estrella. Los médicos se enfrentan a un número creciente de bacterias que se han mostrado resistentes a la mayoría de los antibióticos que están hoy a nuestro alcance. En ocasiones, los médicos deben fiarse de medicamentos caros y de último recurso que acarrean efectos secundarios muy severos. Y todo apunta a que las bacterias también evolucionarán hasta plantar cara a los antibióticos de último recurso. Los médicos están volcados en la tarea de desarrollar nuevos antibióticos, pero puede transcurrir una década desde que se obtenga un medicamento nuevo en el laboratorio hasta que llegue al mercado.
Quizá nos resulte difícil imaginar un mundo en el que no existan los antibióticos, pero ahora debemos imaginarnos un mundo en el que los antibióticos no sean nuestra única arma contra las bacterias. Un siglo después de que D’Herelle se topara por primera vez con los bacteriófagos, puede que estos virus al fin estén listos para ingresar en la medicina moderna.
2015 JAVIER DE LUCAS